题目内容
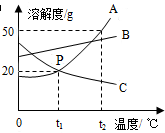 请根据如图中A、B、C三种物质的溶解度曲线,回答下列问题:
请根据如图中A、B、C三种物质的溶解度曲线,回答下列问题:(1)P点的含义是
(2)t2℃时,30gA物质加入到50g水中不断搅拌,能形成80g溶液吗?
(3)将t2℃时的A、B、C三种物质的饱和溶液降温到t1℃时,溶液中溶质质量分数由大到小的顺序是
(4)现有A、B、C三种物质的浓溶液,适用于海水晒盐原理进行结晶的
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)溶解度曲线的交点表示该 温度下两物质的溶解度相等;
(2)据该温度下A的溶解度分析解答;
(3)据饱和溶液中溶质的质量分数计算方法及物质的溶解度随温度变化情况分析解答;
(4)溶解度受温度影响不大的物质适用于海水晒盐原理进行结晶.
(2)据该温度下A的溶解度分析解答;
(3)据饱和溶液中溶质的质量分数计算方法及物质的溶解度随温度变化情况分析解答;
(4)溶解度受温度影响不大的物质适用于海水晒盐原理进行结晶.
解答:解:(1)P点是t1℃时AC的溶解度曲线的交点,二者的溶解度相等;
(2)t2℃时A的溶解度是50g,即100g水中最多溶解50g的A,所以30gA物质加入到50g水中不断搅拌,最多溶解25g,不能形成80g溶液;
(3)由图可知:AB的溶解度随温度升高而增大,C的溶解度随温度升高而减小,所以将t2℃时的A、B、C三种物质的饱和溶液降温到t1℃时,AB析出晶体,依然是饱和溶液,C溶解度变大,溶质的质量分数不变,与降温前相等;据饱和溶液中溶质的质量分数的计算式
×100%可知:溶解度越大质量分数也就越大,而t1℃时B的溶解度大于A的溶解度大于C的溶解度,所以溶液中溶质质量分数由大到小的顺序是 B>A>C;
(4)现有A、B、C三种物质的浓溶液,适用于海水晒盐原理进行结晶的是B,因为B的溶解度受温度影响不大;
故答案为:(1)t1℃时AC的溶解度相等;(2)不能;(3)B>A>C;(4)B.
(2)t2℃时A的溶解度是50g,即100g水中最多溶解50g的A,所以30gA物质加入到50g水中不断搅拌,最多溶解25g,不能形成80g溶液;
(3)由图可知:AB的溶解度随温度升高而增大,C的溶解度随温度升高而减小,所以将t2℃时的A、B、C三种物质的饱和溶液降温到t1℃时,AB析出晶体,依然是饱和溶液,C溶解度变大,溶质的质量分数不变,与降温前相等;据饱和溶液中溶质的质量分数的计算式
| 溶解度 |
| 溶解度+100g |
(4)现有A、B、C三种物质的浓溶液,适用于海水晒盐原理进行结晶的是B,因为B的溶解度受温度影响不大;
故答案为:(1)t1℃时AC的溶解度相等;(2)不能;(3)B>A>C;(4)B.
点评:了解溶解度概念和溶解度曲线的含义,并能灵活应用解答相关问题,溶解度受温度影响不大的物质要从其溶液中得到晶体可采取蒸发溶剂的方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关金属的说法中不正确的是( )
| A、生铁和钢都是铁的合金 |
| B、在铁制品表面刷漆可防锈 |
| C、地壳中含量最多的金属元素是铁元素 |
| D、金属回收和利用是保护金属资源的有效途径 |
如图是初中化学常见的几个实验操作,其中错误的是( )
A、 |
B、 |
C、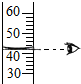 |
D、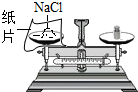 |
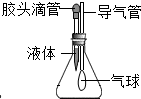 如图所示胶头滴管中是氢氧化钠溶液,锥形瓶中是二氧化碳气体.
如图所示胶头滴管中是氢氧化钠溶液,锥形瓶中是二氧化碳气体.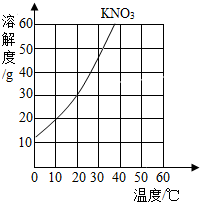 如图是KNO3的溶解度曲线,分析回答问题.
如图是KNO3的溶解度曲线,分析回答问题.