题目内容
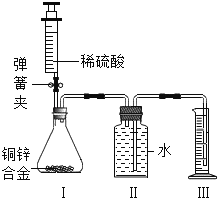
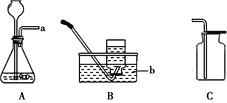
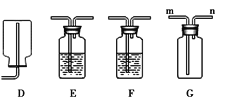
【题目】现有如图所示的下列实验装置,根据下图所示,回答下面问题。
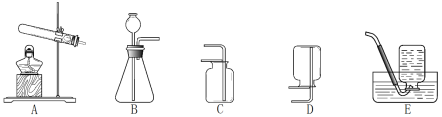
(1)实验室用高锰酸钾制取氧气应选用的发生装置是________,(填字母代号,下同)反应的文字表达式为___________。若要收集一瓶干燥的氧气应选用收集装置为_________。若用E装置收集氧气的最佳时间是_____。
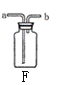
(2)若实验室改用B装置来制取氧气,应选用的药品是_____,反应的文字表达式为_________;检验O2已收集满的方法是___________。若用F装置收集氧气,气体应从______端通入(填a或b),铁丝在氧气中燃烧为什么集气瓶底装一层水或细沙________
【答案】A 高锰酸钾![]() 锰酸钾+二氧化锰+氧气 C 气泡均匀连续 过氧化氢溶液和二氧化锰 过氧化氢
锰酸钾+二氧化锰+氧气 C 气泡均匀连续 过氧化氢溶液和二氧化锰 过氧化氢![]() 水+氧气 将带火星的木条放在集气瓶口部,木条复燃,则氧气收集满 a 防止生成物溅落瓶底,使集气瓶炸裂
水+氧气 将带火星的木条放在集气瓶口部,木条复燃,则氧气收集满 a 防止生成物溅落瓶底,使集气瓶炸裂
【解析】
(1)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,对应的文字表达式为:高锰酸钾![]() 锰酸钾+二氧化锰+氧气,是固体加热条件下制取气体,所以发生装置为A。若要收集干燥的气体则不能用排水法,而氧气的密度大于空气,所以用向上排空气法,故选C。若用E收集氧气,最佳的收集时间是气泡均匀连续的时候,此时已经排空装置内的空气。
锰酸钾+二氧化锰+氧气,是固体加热条件下制取气体,所以发生装置为A。若要收集干燥的气体则不能用排水法,而氧气的密度大于空气,所以用向上排空气法,故选C。若用E收集氧气,最佳的收集时间是气泡均匀连续的时候,此时已经排空装置内的空气。
(2)若用B装置制取氧气,为常温下固液反应,药品为过氧化氢溶液和二氧化锰,对应的文字表达式为:过氧化氢![]() 水+氧气。验满是将带火星的木条放在集气瓶口,木条复燃,则氧气收集满;若用F装置收集氧气,由于氧气的密度比空气大,所以气体应从a端通入。集气瓶底部放少量水或细沙的作用是防止生成物溅落瓶底,使集气瓶炸裂。
水+氧气。验满是将带火星的木条放在集气瓶口,木条复燃,则氧气收集满;若用F装置收集氧气,由于氧气的密度比空气大,所以气体应从a端通入。集气瓶底部放少量水或细沙的作用是防止生成物溅落瓶底,使集气瓶炸裂。

练习册系列答案
相关题目