题目内容
【题目】(5分)甲、乙两种固体物质的溶解度曲线如图Ⅰ所示。常温下,分别向装有适量甲、乙物质的两支试管里加入等量的蒸馏水,充分振荡后,两支试管底部均有未溶解的固体;再将两支试管放入盛有冰水混合物的烧杯里,如图Ⅱ所示。
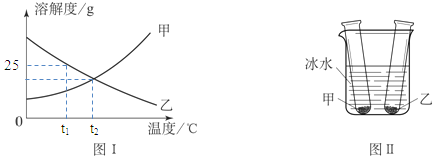
(1)t1℃时,乙物质的饱和溶液的溶质质量分数 25%(填“>”、“<”、“=”之一)。
(2)t2℃时,甲物质的溶解度 乙物质的溶解度(填“>”、“<”、“=”之一)。
(3)若甲中含有少量的杂质乙,可采用 方法提纯甲。(填“蒸发结晶”、“降温结晶”之一)
(4)在图Ⅱ实验中看到的实验现象是甲试管中固体增多,乙两试管里固体减少。请你对此现象作出解释。 。
【答案】(1)<;(2)=;(3)降温结晶;(4)温度降低,甲物质的溶解度减小,饱和溶液中析出固体,固体增多;乙物质的溶解度增大,固体减少。
【解析】
试题分析:(1)t1℃时,乙物质的溶解度为25g;即在t1℃时,在100g水中溶解乙物质25g即可达到饱和。所以其饱和溶液的溶质质量分数为![]() ×100%=20%<25%;
×100%=20%<25%;
(2)根据图示可知:t2℃时,甲物质的溶解度等于乙物质的溶解度。
(3)根据图示可知:甲的溶解度随着温度的降低而减小,而乙的溶解度温度的降低而增大;即当降温时甲的饱和溶液中会析出甲;而乙不会析出。所以若甲中含有少量的杂质乙,可采用降温结晶方法提纯甲。
(4)“甲试管中固体增多,乙两试管里固体减少”说明当温度降低时,甲物质的溶解度减小,原饱和溶液中的溶质无法完全溶解,会析出固体,固体增多;乙物质的溶解度增大,饱和溶液成为不饱和溶液,固体会继续溶解一部分,固体减少。

 阅读快车系列答案
阅读快车系列答案【题目】对下列生话中的现象或做法的解释正确的是
事 实 | 解 释 | |
A. | 蜡烛一吹就熄 | 吹出的CO2隔绝了氧气 |
B. | 热胀冷缩 | 分子间空隙随温度的改变而改变 |
C. | 食盐水可以导电 | 溶液中有自由移动的分子 |
D. | 伍德合金可作为保险丝 | 合金的熔点比其组成金属高 |