题目内容
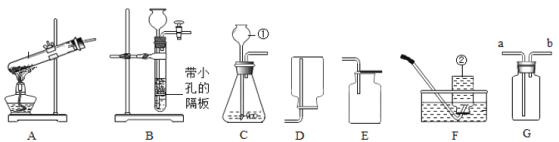
【题目】如图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题:

(1)描述A中的实验现象________ .
(2)B中的实验现象________ .
(3)写出C中反应的化学方程式________ .
(4)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是 ________ (填字母).
【答案】铜丝表面附着了一层银白色固体,溶液由无色变成蓝色 铁丝表面附着了一层红色固体,溶液由蓝色变成浅绿色 Zn+2HCl=ZnCl2+H2↑ AB
【解析】
根据金属活动性顺序可知,金属活动性强弱依次是锌、铁、氢、铜、银,4个实验均能发生反应。
(1)A中铜和硝酸银反应生成银和硝酸铜,实验现象铜丝表面附着了一层银白色固体,溶液由无色变成蓝色。
(2)B中铁和硫酸铜反应生成铜和硫酸亚铁,实验现象铁丝表面附着了一层红色固体,溶液由蓝色变成浅绿色。
(3)C中锌和盐酸反应生成氢气和氯化锌,反应的化学方程式Zn+2HCl=ZnCl2+H2↑ 。
(4)A中铜和硝酸银反应生成银和硝酸铜,证明铜比银强;B中铁和硫酸铜反应生成铜和硫酸亚铁,证明铁比铜强,AB能够证明金属活动性由强到弱依次是Fe、Cu、Ag,至少要做的实验是AB。

 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案【题目】根据实验内容选择最恰当选项完成下列实验记录(填写字母)
(1)用试管将水加热至沸腾。把一块洁净的玻璃片移近试管口,观察并记录发生的现象
(2)如图所示,在盛有少量石灰石的试管中,加入适量稀盐酸。注意观察并记录两支试管中发生的变化。
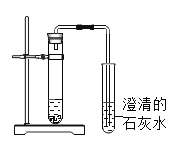
实验现象有:
A 产生大量无色气体 B 水沸腾变成蒸气
C 澄清石灰水变浑浊 D 蒸气遇冷的玻璃片凝结成无色液滴
实验序号 | 变化前的物质 | 变化时发生的现象 | 变化后的物质 |
(1) | 液态的水 | _____ | 液态的水 |
(2) | 块状的石灰石等 | _____ | 二氧化碳气体等 |