题目内容
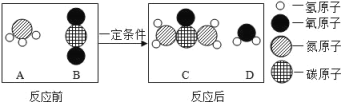
【题目】硝酸制备中会发生反应4NH3+5O2=4X+6H2O.下列说法正确的是( )
A. 反应消耗氧与生成水中氧的质量比为5:3
B. X的化学式为NO2
C. 该反应过程中元素化合价均没有发生变化
D. NH3中氮的质量分数为25%
【答案】A
【解析】
A、根据化学方程式可知,反应消耗氧气与生成水中氧元素的质量比为![]() ,故A正确。
,故A正确。
B、由反应的化学方程式4NH3+5O2═4X+6H2O,反应前氮、氢、氧原子个数分别为4、12、10,反应后的生成物中氮、氢、氧原子个数分别为0、12、6,根据反应前后原子种类、数目不变,则4X分子中含有4个氮原子和4个氧原子,则每个X分子由1个氮原子和1个氧原子构成,物质X的化学式为NO,故B错误;
C、反应物中氧气是单质,单质中元素的化合价为0,生成物NO和H2O中的氧元素化合价为-2价,该反应过程中氧元素化合价一定会发生变化,故C错误;
D、NH3中氮的质量分数=![]() ,故D错误。故选A。
,故D错误。故选A。

【题目】某化学兴趣小组的同学在整理化学药品柜时,发现有一瓶标签受损的无色溶液(受损标签如图所示)。咨询实验室老师得知,这瓶无色溶液是一种常用的盐溶液,小组同学对这瓶溶液进行了如下探究:

提出问题:这瓶无色溶液是什么物质的溶液?
猜想与假设:小组同学提出了如下假设
①碳酸钠溶液 ②硫酸钠溶液 ③氯化钠溶液
讨论交流 在老师的指导下,小组同学经过讨论,认为第______条假设不合理。请你说明不合理的理由:____________;
查阅资料:硫酸钡既不溶于水又不溶解于酸;碳酸钠溶液呈碱性;
Ba(OH)2的化学性质与Ca(OH)2相似。
进行实验 小组同学设计并进行了如下实验,请你完善小组同学的“相互评价”。
组次 | 实验操作 | 出现的现象与结论 | 同学相互评价 |
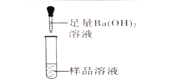
1 |
| 产生白色沉淀, 第1组同学认为猜想②成立 | 第2组同学认为此方案结论不正确。你认为其理由是硫酸钡和______都不溶于水 |
2 |
| 试管中无明显现象, 第2组同学认为猜想②成立 | 第3组同学认为此方案结论不正确。你认为其理由是________________。 |
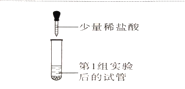
3 |
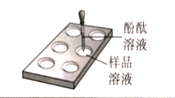
| 溶液无明显变化, 第3组同学认为猜想②成立 | 第1组同学认为此方案结论正确。你认为实验中用点滴板比试管具有更多的优点的是_______(写一条即可) |
原理分析 猜想②正确,写出第一组实验的化学方程式______
实验反思 针对上述情况,小组同学总结了取用药品时各种注意事项,你认为倾倒液体药品时,要注意__________。