题目内容
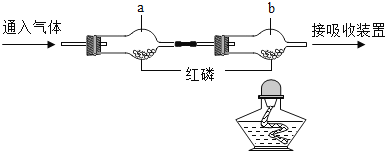
【题目】资料显示,将新制的浓度为5%的过氧化氢溶液,加热到80℃ 时,才有较多氧气产生。 而相同质量的5%的过氧化氢溶液加入二氧化锰,常温下就会立即产生氧气,因此实验室多用此方法制氧气。
(1)写出实验室里以过氧化氢溶液为原料制氧气的符号表达式___________。
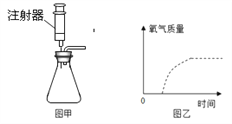
(2)利用图甲装置可作为上述反应的发生装置,则注射器的作用是_______。
(3)分别采用两份相同质量且浓度均为5%的过氧化氢溶液制氧气,图乙虚线表示加热分解制取氧气的曲线,请你在该图中用实线画出加入二氧化锰制取氧气的大致曲线 (假定两种方法过氧化氢均完全分解;曲线画在答题纸上):___________。
(4)小芳查阅资料,发现除二氧化锰外,某些物质也可以作为过氧化氢溶液分解的催化剂。
【提出猜想】除二氧化锰外,氧化铜也可以作过氧化氢溶液分解的催化剂。
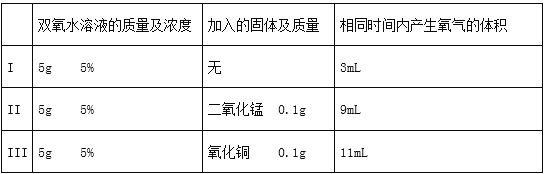
【完成实验】按下表进行实验,实验数据记录如下:
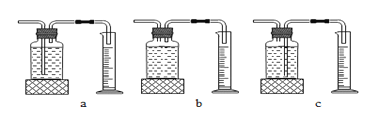
本实验中,测量氧气体积的装置应选择____________(填序号)。
【数据分析】由实验__________与实验III对比,证明氧化铜也可加快过氧化氢溶液分解的速率;
若要进一步证明氧化铜确实是该反应的催化剂,则还需要验证它在反应前后____和_____不变。
【答案】 H2O2 ![]() H2O+O2 便于控制滴加液体的速率 ,从而控制化学反应的速率
H2O+O2 便于控制滴加液体的速率 ,从而控制化学反应的速率 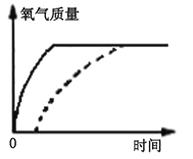 c I 质量(或化学性质) 化学性质(或质量)
c I 质量(或化学性质) 化学性质(或质量)
【解析】本题考查了实验室制氧气的装置和探究催化剂的特点。催化剂的特点是“一变,两不变”,即能改变化学反应的速率,而本身的质量和化学性质不变。
(1)过氧化氢在二氧化锰的催化作用下分解为水和氧气,符号表达式是H2O2 ![]() H2O+O2;
H2O+O2;
(2)注射器便于控制滴加液体的速率,从而控制反应的速率;
(3)由于过氧化氢溶液加入二氧化锰,常温下就会立即产生氧气,所以曲线的起点应从原点开始,二氧化锰在反应中用作催化剂,能改变反应速率但不能改氧气的生成量,所以生成氧气的质量与加热生成的氧气质量相同。加入二氧化锰制取氧气的大致曲线如下图: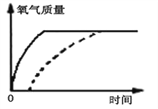
(4)由于氧气的密度小于水的密度,所以实验中测量O2体积的装置应该选择c;
数据分析:将没有加入其他物质的一组与加入氧化铜的一组进行对比,比较氧化铜是否可以加快过氧化氢的分解速率,故答案为:实验I;催化剂是指在化学反应中能改变其他物质的化学反应速度而本身的质量和化学性质都不发生改变的物质,该实验已证明氧化铜也可加快过氧化氢溶液分解的速率,还需验证它在反应前后质量和化学性质不变。

 名校课堂系列答案
名校课堂系列答案