题目内容
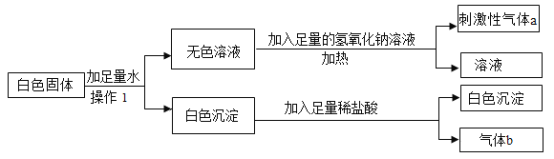
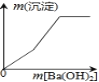
【题目】请根据如图所示的实验过程和提供的数据,回答下列问题:
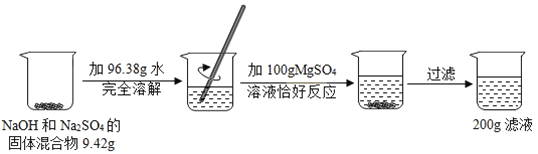
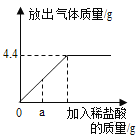
(1)实验过程中,产生沉淀的质量为______g。
(2)最终所得溶液的溶质质量分数为多少?(写出计算过程)________________
(3)原固体混合物中钠元素的质量为______g。
【答案】5.8 7.81% 5.06
【解析】
氢氧化钠和硫酸镁反应生成硫酸钠和氢氧化镁沉淀。
(1)实验过程中二者恰好反应,根据质量守恒定律可知,产生沉淀的质量为![]() 。
。
(2)设混合物中氢氧化钠的质量为x,生成硫酸钠的质量为y ![]()
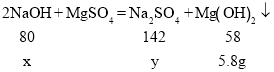
![]()
![]()
则反应后所得溶液中硫酸钠的质量为![]()
则硫酸钠溶液的溶质质量分数为![]()
(3)化学反应前后元素的质量不变,所以原固体混合物中钠元素的质量与最后溶液中钠元素的质量相等,最后溶液中只有溶质![]() ,所以钠元素质量为
,所以钠元素质量为![]() 。
。
答:实验过程中,产生沉淀的质量为5.8g,最终所得溶液的溶质质量分数为7.81%,原固体混合物中钠元素的质量为5.06g。

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目