题目内容
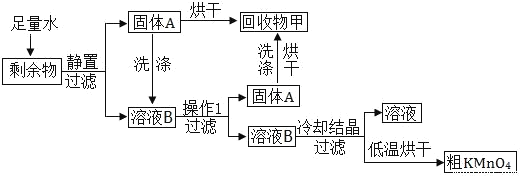
【题目】雾霾严重影响人们的生活和健康。某地区的雾霾中可能含有如下可溶性物质NH4NO3、NaNO3、BaCl2、MgCl2、Na2SO4。某同学收集了该地区的雾霾,经必要的处理后得到试样溶液,设计并完成了下图所示实验。请根据实验操作与现象回答:
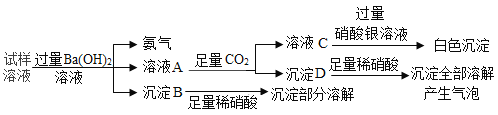
(1)沉淀B的化学式为___________。
(2)产生沉淀D的化学方程式为___________。
(3)试样溶液中一定含有___________,可能含有___________ ,一定不含___________。
【答案】Mg(OH)2、BaSO4 Ba(OH)2+CO2=BaCO3↓+H2O NH4NO3、MgCl2、Na2SO4 NaNO3 BaCl2
【解析】
铵根离子与氢氧根离子结合能生成氨气。试样溶液中加入过量Ba(OH)2生成氨气,则试样中含有铵根离子;加入过量Ba(OH)2溶液后产生沉淀B,且沉淀B加入足量稀硝酸后部分溶解,氢氧化镁能与稀硝酸反应生成可溶性硝酸镁和水,硫酸钡不溶于稀硝酸,推断试样中含有MgCl2和Na2SO4,其中MgCl2和Ba(OH)2反应生成溶于酸的Mg(OH)2,Na2SO4和Ba(OH)2反应生成不溶于酸的BaSO4,由于Na2SO4与BaCl2不能共存,故BaCl2一定不存在;向溶液A中通入二氧化碳得到溶液C、沉淀D,溶液C中加入硝酸银溶液,生成白色沉淀,说明含有氯离子;沉淀D即为二氧化碳与过量氢氧化钡溶液反应生成的碳酸钡沉淀。
(1)根据以上分析可知:B是氢氧化镁和硫酸钡,化学式分别为:Mg(OH)2、BaSO4;
(2)产生沉淀D是氢氧化钡与二氧化碳反应生成碳酸钡沉淀和水,反应的化学方程式为:Ba(OH)2+CO2=BaCO3↓+H2O;
(3)试样中一定含有硝酸铵、氯化镁、硫酸钠,可能含有硝酸钠,一定不含有氯化钡,故填:NH4NO3、MgCl2、Na2SO4;NaNO3;BaCl2

 名校课堂系列答案
名校课堂系列答案