题目内容
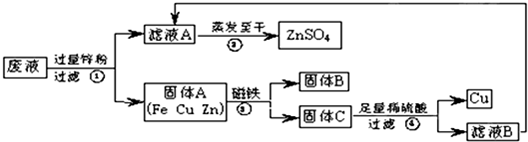
28、实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放就会造成水污染.于是几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属.实验过程如下:

请回答:
(1)滤液A和滤液B含有相同的溶质,其名称是
(2)写出步骤①其中一个反应的化学方程式
步骤④发生反应的化学方程式为
(3)要检验步骤④中加入的稀硫酸是否足量的方法是
(4)若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量:废液的质量和

请回答:
(1)滤液A和滤液B含有相同的溶质,其名称是
硫酸锌
;固体B的化学式为Fe
.(2)写出步骤①其中一个反应的化学方程式
Zn+CuSO4=ZnSO4+Cu
;步骤④发生反应的化学方程式为
Zn+FeSO4═ZnSO4+Fe Zn+H2SO4=ZnSO4+H2↑
.(3)要检验步骤④中加入的稀硫酸是否足量的方法是
取步骤④的滤渣于试管中加入少量稀硫酸,若有气泡产生则酸不足量(或若无气泡产生,则酸已足量)
.(4)若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量:废液的质量和
硫酸锌的质量、锌粉的质量
.分析:(1)由题意可知:②中蒸发至干,得硫酸锌;因为滤液A和滤液B含有相同的溶质,所以步骤④中加入的稀硫酸,得硫酸锌;
(2)根据题中的信息,推导出反应物和生产物,正确书写化学方程式;
(3)检验加入的稀硫酸是否足量:取步骤④的滤渣于试管中加入少量稀硫酸,若有气泡产生则酸不足量(或若无气泡产生,则酸已足量),即铁与稀硫酸反应;
(4)若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量:废液的质量和硫酸锌的质量、锌粉的质量.
(2)根据题中的信息,推导出反应物和生产物,正确书写化学方程式;
(3)检验加入的稀硫酸是否足量:取步骤④的滤渣于试管中加入少量稀硫酸,若有气泡产生则酸不足量(或若无气泡产生,则酸已足量),即铁与稀硫酸反应;
(4)若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量:废液的质量和硫酸锌的质量、锌粉的质量.
解答:解:(1)利用金属活动性顺序,回收工业重要原料硫酸锌和有关金属; 故答为:硫酸锌,铁
(2)根据题中的信息,推导出反应物和生产物,利用金属活动性顺序,正确书写化学方程式; 故答为:Zn+CuSO4=ZnSO4+Cu
Zn+FeSO4═ZnSO4+Fe Zn+H2SO4=ZnSO4+H2↑
(3)检验加入的稀硫酸是否足量:取步骤④的滤渣于试管中加入少量稀硫酸,若有气泡产生则酸不足量(或若无气泡产生,则酸已足量),即由题意可推知铁与稀硫酸反应; 故答为:取步骤④的滤渣于试管中加入少量稀硫酸,看是否有气泡产生.
(4)若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量:废液的质量和硫酸锌的质量、锌粉的质量.
故答为:硫酸锌的质量、锌粉的质量.
(2)根据题中的信息,推导出反应物和生产物,利用金属活动性顺序,正确书写化学方程式; 故答为:Zn+CuSO4=ZnSO4+Cu
Zn+FeSO4═ZnSO4+Fe Zn+H2SO4=ZnSO4+H2↑
(3)检验加入的稀硫酸是否足量:取步骤④的滤渣于试管中加入少量稀硫酸,若有气泡产生则酸不足量(或若无气泡产生,则酸已足量),即由题意可推知铁与稀硫酸反应; 故答为:取步骤④的滤渣于试管中加入少量稀硫酸,看是否有气泡产生.
(4)若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量:废液的质量和硫酸锌的质量、锌粉的质量.
故答为:硫酸锌的质量、锌粉的质量.
点评:仔细审题,有题意可知一些信息,根据信息推导做题;利用金属活动性顺序,回收工业重要原料硫酸锌和有关金属.

练习册系列答案
相关题目