题目内容
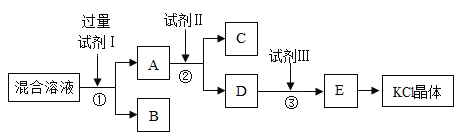
【题目】甲、乙、丙为初中化学常见的三种物质,它们之间的转化转化关系、反应 条件部分如图所示(图中反应物和生成物已略去)。
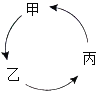
(1)若甲为葡萄糖(C6H12O6),丙是最常用溶剂,则自然界吸收 乙气体的主要途径是_____,乙转化成丙的化学方程式 为_____。
(2)甲、乙、丙均为钙的化合物,且甲为氧化物,则甲的名称是_____, 丙转化成甲的化学方程式为_____。
【答案】光合作用 CO2+Ca(OH)2=CaCO3↓+H2O 氧化钙 CaCO3 ![]() CaO+CO2↑
CaO+CO2↑
【解析】
(1)若甲为葡萄糖(C6H12O6),丙是最常用溶剂,则丙是水;葡萄糖在人体能氧化生成二氧化碳,二氧化碳与氢氧化钙反应产生碳酸钙和水,乙可能是二氧化碳气体,自然界吸收二氧化碳气体的主要途径是:光合作用,二氧化碳与氢氧化钙反应产生碳酸钙和水的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
(2)甲、乙、丙均为钙的化合物,且甲为氧化物,则甲的名称是氧化钙, 氧化钙与水反应产生氢氧化钙,则乙是氢氧化钙,氢氧化钙与二氧化碳反应产生碳酸钙,碳酸钙高温分解产生氧化钙和二氧化碳气的化学方程式为:CaCO3 ![]() CaO+CO2↑。
CaO+CO2↑。

练习册系列答案
相关题目
【题目】如图所示是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷,将它放在盛有沸水的烧杯上方进行实验。请完成下表中的空白:(提示:白磷与红磷类似,燃烧都生成五氧化二磷,但是白磷燃烧所需达到的温度只有40C)
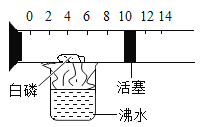
实验目的 | 实验现象 | 实验结论 |
测定空气中______ 的体积分数 | 白磷着火燃烧,活塞先右移,后左移,最后停在刻度约为___________(填整数)的位置上 | 空气的成分按体积计算, ________约占l/5 |