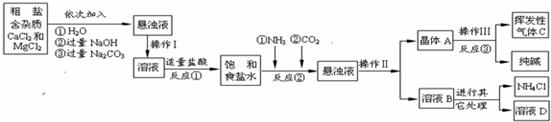
题目内容
已知在20℃时,氯化钠的溶解度为36g,20℃时将18g氯化钠溶于32g水中,所得溶液中溶质的质量分数为
[ ]
A.18%
B.36%
C.26.5%
D.无法计算
B.36%
C.26.5%
D.无法计算
C

练习册系列答案
相关题目
(一)某工厂以流量为Q1排出含硫酸a%的工业废水,现在往该废水中注入含氢氧化钠b%的工业废水将其酸性中和后再排出.要使处理后的废水pH约为7,求氢氧化钠溶液的流量Q2(结果用分式表示).(已知:Q1、Q2代表单位时间流经溶液的体积,且含酸废水的密度和含碱废水的密度均为ρ)
(备用)(必要时用于提高难度))
(二)东方中学课外活动小组在测定由氯化钠和硫酸钠形成混合物的组成时,进行了以下实验:取20g混合物全部溶于水,将得到的溶液等分为4份,然后分别加入一定量未知质量分数的氯化钡溶液,实验数据见下表:
若有关的化学反应为:Na2SO4+BaCl2=BaSO4↓+2NaCl,请计算:
(1)未知氯化钡溶液的质量分数为多少.
(2)原混合物中硫酸钠的质量分数是多少.(精确到0.01)
(备用)(必要时用于提高难度))
(二)东方中学课外活动小组在测定由氯化钠和硫酸钠形成混合物的组成时,进行了以下实验:取20g混合物全部溶于水,将得到的溶液等分为4份,然后分别加入一定量未知质量分数的氯化钡溶液,实验数据见下表:
| 第一份 | 第二份 | 第三份 | 第四份 | |
| 加入氯化钡溶液质量(g) | 15 | 20 | 25 | 30 |
| 反应得到沉淀的质量(g) | 1.40 | 1.86 | 2.33 | 2.33 |
(1)未知氯化钡溶液的质量分数为多少.
(2)原混合物中硫酸钠的质量分数是多少.(精确到0.01)
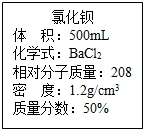 实验室有一瓶浓氯化钡溶液,瓶上标签内容如图所示,请你根据标签上提供的数据解答下列问题.我市某中学课外活动小组在测定RCl和R2S04形成混合物的百分组成时(R代表某金属元素).进行了以下实验.
实验室有一瓶浓氯化钡溶液,瓶上标签内容如图所示,请你根据标签上提供的数据解答下列问题.我市某中学课外活动小组在测定RCl和R2S04形成混合物的百分组成时(R代表某金属元素).进行了以下实验.