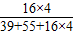题目内容
为得知15.8g高锰酸钾完全分解能产生多少克氧气,甲、乙两同学分别采取了以下方法:
(1)甲同学的方法(实验法).
将15.8g高锰酸钾充分加热,测得生成氧气的体积为1300mL.
(2)乙同学的方法(计算法)
高锰酸钾中氧元素的质量分数
=
×100%
=
=40.5%
生成氧气的质量为:15.8g×40.5%=6.4g
答:(略)
请回答:
(1)甲同学实验制得的氧气,约相当于相同条件下______mL空气中所含的氧气.(精确到l mL)
(2)经过讨论,大家认为乙的计算方法明显错误,本题不能采用该方法计算氧气质量的理由是______.(填字母)
A.高锰酸钾中含氧元素 B.锰酸钾和二氧化锰中含氧元素 C.氧气中含氧元素
(3)请用正确的方法计算15.8g高锰酸钾完全分解所产生的氧气的体积是多少毫升?(已知在实验条件下,氧气的密度为1.4g/L.结果精确到l mL.)
(4)若实验操作无错误,则甲同学的实验结果比理论值偏大的原因可能是______(说出一点即可).
(1)甲同学的方法(实验法).
将15.8g高锰酸钾充分加热,测得生成氧气的体积为1300mL.
(2)乙同学的方法(计算法)
高锰酸钾中氧元素的质量分数
=
| O的相对原子质量 |
| KMnO4的相对分子质量 |
=
| 16×4 |
| 39+55+16×4 |
=40.5%
生成氧气的质量为:15.8g×40.5%=6.4g
答:(略)
请回答:
(1)甲同学实验制得的氧气,约相当于相同条件下______mL空气中所含的氧气.(精确到l mL)
(2)经过讨论,大家认为乙的计算方法明显错误,本题不能采用该方法计算氧气质量的理由是______.(填字母)
A.高锰酸钾中含氧元素 B.锰酸钾和二氧化锰中含氧元素 C.氧气中含氧元素
(3)请用正确的方法计算15.8g高锰酸钾完全分解所产生的氧气的体积是多少毫升?(已知在实验条件下,氧气的密度为1.4g/L.结果精确到l mL.)
(4)若实验操作无错误,则甲同学的实验结果比理论值偏大的原因可能是______(说出一点即可).
(1)空气的体积为:1300mL÷
═6500mL
故答案为:6500
(2)计算出的质量是高锰酸钾中的氧元素的质量,包括了生成的锰酸钾和二氧化锰中氧元素的质量.
故选B
(3)设生成氧气的质量为x.
2KMnO4
K2MnO4+MnO2+O2↑
316 32
15.8g x
=
,
x=1.6g
实验条件下氧气的体积为
=1.143L
答:产生的氧气的体积为1.143L
(4)实际测得的氧气的质量大于理论计算出的氧气的质量,原因可能是生成锰酸钾或二氧化锰分解放出了氧气.
故答案为:可能是生成锰酸钾或二氧化锰分解放出了氧气.
| 1 |
| 5 |
故答案为:6500
(2)计算出的质量是高锰酸钾中的氧元素的质量,包括了生成的锰酸钾和二氧化锰中氧元素的质量.
故选B
(3)设生成氧气的质量为x.
2KMnO4
| ||
316 32
15.8g x
| 316 |
| 15.8g |
| 32 |
| x |
x=1.6g
实验条件下氧气的体积为
| 1.6g |
| 1.4g/L |
答:产生的氧气的体积为1.143L
(4)实际测得的氧气的质量大于理论计算出的氧气的质量,原因可能是生成锰酸钾或二氧化锰分解放出了氧气.
故答案为:可能是生成锰酸钾或二氧化锰分解放出了氧气.

练习册系列答案
 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
解决问题常面临着方法的选择,面对不同的结果我们应继续探索。为得知15.8g高锰酸钾完全分解能产生多少克氧气,小柯与小妍分别采取了以下方法:
| 小柯:实验测定法 | 小妍:计算法 |
| 小柯在老师的指导下,将15.8g高锰酸钾充分加热,得到氧气1300ml. | 解:高锰酸钾中氧元素的质量分数 O的相对原子×4 = ——————————×100% KMnO4的相对分子质量 16×4 = ——————————×100%=40.5% 39+55+16×4 氧气的质量为:15.8g×40.5%=6.40g 答:15.8个高锰酸钾完全分解产生氧气6.4g. |
请回答:
⑴在本实验条件下,氧气的密度为1.4×10-3g/mL,则由小柯的测量结果可算出15.8g高锰酸钾分解后所产生的氧气质量为 g.
⑵大家经过讨论,认为小妍的计算方法明显错误,此题不能采用该方法计算氧气质量的一项理由是 。
A.高锰酸钾中含氧元素
B.锰酸钾和二氧化锰中含氧元素
C.氧气中含氧元素
⑶请计算15.8g高锰酸钾完全分解所产生的氧气质量。
⑷若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,请提出一种合理的猜测: 。
 ×100%
×100%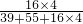
 ×100%
×100%