题目内容
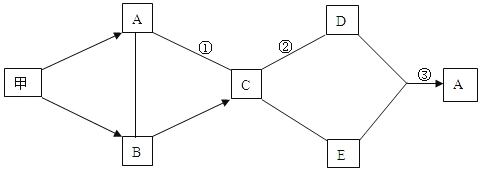
【题目】如图是初中化学中常见物质间的转化关系,其中只有甲为单质,其他都是化合物; A是植物进行光合作用的一种重要原料,C可用于中和酸性土壤,反应②属于中和反应,其余反应条件、部分反应物和生成物已略去,试推断:
(1)B物质的化学式_______;E物质的类别是_________。
(2)写出下列化学方程式:甲→B:_________。反应③:________。
【答案】H2O 盐 2H2+O2![]() 2H2O Na2CO3+2HCl═2NaCl+H2O+CO2↑(或其他合理答案)
2H2O Na2CO3+2HCl═2NaCl+H2O+CO2↑(或其他合理答案)
【解析】
(1)A是光合作用的原料,则它会是水或二氧化碳中的一种,而C能中和土壤中的酸,则C是氢氧化钙,且它能与A反应,则A应该是二氧化碳,利用这一突破口可解决此题;
(2)氧气可以生成二氧化碳,二氧化碳和水反应生成碳酸,水和氧化钙反应生成氢氧化钙,则B是水,故甲是氧气;碳酸钠与氢氧化钙的反应,和酸反应生成二氧化碳,所以E是碳酸盐如碳酸钠。
(1))B是水, E属于碳酸盐,故答案为:H2O;盐;
(2)甲→B是氢气和氧气反应生成水,甲→B的反应方程式为:2H2+O2![]() 2H2O,反应③是盐酸和碳酸钠反应生成氯化钠、水、二氧化碳,化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑(或其他合理答案)。
2H2O,反应③是盐酸和碳酸钠反应生成氯化钠、水、二氧化碳,化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑(或其他合理答案)。

【题目】过氧化钠是化学中常见的一种药品,它是浅黄白色颗粒粉末.在空气中吸收水分和二氧化碳。易溶于水,与水中能发生反应生成氢氧化钠和过氧化氢,方程式:Na2O2+2H2O=2NaOH+H2O2,过氧化氢又能分解放出氧气。
(1)区分水和过氧化氢的实验方法是:___________________________,发生的反应方程式是:__________________________.
(2)某同学为了证明过氧化钠加入水中生成了氢氧化钠,在生成的溶液中滴加了几滴无色酚酞试液,观察到的现象是溶液先变红后褪为无色,请你对此现象进行探究.
提出问题:什么导致溶液先变红再褪色?
猜想与假设:
猜想1:甲同学“可能是无色酚酞溶液变质导致溶液褪色”;
猜想2:乙同学“可能是生成的过氧化氢使溶液褪色”.
实验与结论:
a:甲同学提出的猜想,立即遭到其他同学的反对,因为______________________________;
b:为了验证自己的猜想,乙同学设计了以下方案并实验验证:
实验步骤 | 实验现象 | 实验结论 |
取少量稀氢氧化钠溶液于试管中,滴加1﹣2滴酚酞试液,变红后,___________观察现象 | 溶液依然为红色 | ____________________ |
讨论交流:你还能提出不同的猜想吗?如果还能提出新的合理的假设和方案你将获得奖励分4分.
猜想3:_____________
方案3:
实验步骤 | 实验现象 | 实验结论 |
_________________ | _______________ | ______________ |