��Ŀ����
����Ŀ��ʵ������һƿ�����Һ����ʦ��С��ͬѧ��Ʒ����ⶨ�÷�Һ�����������������С��ͬѧ��ȡһ����С�ձ�����������Ϊ18.2g��Ȼ�������е������������Һ�������������Ϊ33.2g��֮��һö����Ϊ10.8g������������ɰֽɰȥ���⣩�����С�ձ��з�Ӧ�����������治�������ݲ������ٴγ�����������Ϊ43.9g����ش��������⣺
��1����Ӧ�в���������������� ��
��2������÷�Һ�����������������д��������̣�����������һλС������
��3���������������δ�������ԣ�2����������Ӱ���� ��ѡ�ƫ����ƫС��������Ӱ�족����ԭ���� ��
���𰸡�0.1g����������Ӧ�����������Ϊx
Fe+H2SO4�TFeSO4+H2��
98 2
X0.1g
![]() x=4.9g��
x=4.9g��
�÷�Һ���������������Ϊ��![]() ��100%=32.7%���𣺷�Һ�����������������32.7%��
��100%=32.7%���𣺷�Һ�����������������32.7%��
ƫС������Ҳ������һ�������ᡣ
��������
�������������ϡ���ᷴӦ�������������������������ϡ���ᷴӦ������������ˮ��������������������������������������е����ʵ������������������������������������Ϊ��33.2g+10.8g��43.9g=0.1g����������Ӧ�����������Ϊx����ϻ�ѧ����ʽ��������������С�ձ���ϡ�����Һ������Ϊ��33.2g��18.2g=15.0g���������������������㹫ʽ������ã��������������δ����������������һ�������ᣬ�����������������������ƫС���Ӷ�ʹ��������������������ƫС��

 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�����Ŀ�� KNO3��KCl�ڲ�ͬ�¶�ʱ���ܽ�����±���ʾ����ش��������⣺
�¶�/�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
�ܽ��/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
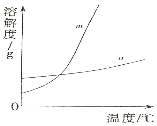
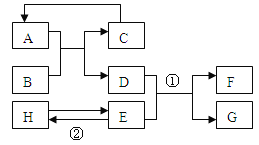
��1�������ϱ����ݣ�����KNO3��KCl���ܽ�����ߣ���ͼ���ܱ�ʾKNO3�ܽ�����ߵ��� �� ������m��n��
��2���ɱ������ݷ�����֪�� KNO3��KCl��ijһ�¶�ʱ������ͬ���ܽ��x����x��ֵ�� �� ��
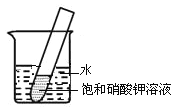
��3������ͼ��ʾ��20��ʱ����ʢ�б���KNO3��Һ��С�Թܷ���ʢˮ���ձ��У���ˮ�м���ij���ʺ��Թ����о�����������������ʿ����������е�___��_____������ĸ��ţ���
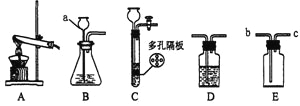
A���������ƹ��� B����ʯ�ҹ��� C������ D������粒��� E��Ũ����