题目内容
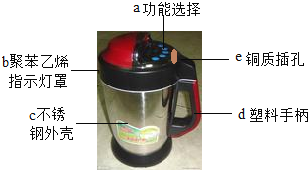
【题目】如图是家用豆浆机,请根据图回答下列问题:
(1)制作材料中属于金属或合金的是_____(选填一种物质编号)。
(2)属于有机合成材料的是_____(选填一种物质编号)。
(3)制作材料中含有的金属单质的化学式是_____。
(4)将豆渣和豆浆分离的方法类似于我们实验中的_____操作。
(5)证明大豆粉富含蛋白质的方法是_____。
(6)制作材料中的铜能与浓硝酸反应,反应的化学方程式为![]() ,X 的化学式为_____。
,X 的化学式为_____。
【答案】c或e b或d Cu 过滤 取少量大豆粉灼烧,闻其是否有烧焦羽毛的气味,有则含蛋白质,无则不含蛋白质 NO2
【解析】
(1)合金是指金属与其他金属或非金属熔合一起得到的具有金属性能的一类材料,制作材料中属于金属或合金的是:铜或不锈钢,故选c或e;
(2)合成材料却是指利用化学反应合成而得到的一些材料,故选b或d。
(3)制作材料中含有的金属单质是铜,其化学式是Cu;
(4)把不溶于液体的固体物质与液体分离开来的方法叫作过滤;将豆渣和豆浆分离的方法类似于我们实验中的过滤操作;
(5)证明大豆粉富含蛋白质的方法是:取少量大豆粉灼烧,闻其是否有烧焦羽毛的气味,有则含蛋白质,无则不含蛋白质;
(6)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式![]() ,反应前铜、氢、氮、氧原子数目分别为1、4、4、12,反应后的生成物中铜、氢、氮、氧原子数目分别为1、4、2、8,根据反应前后原子种类、数目不变则2X分子中含有2个氮原子和4个氧原子,则每个X分子由1个氨原子和2个氧原子构成,则物质X的化学式为NO2。
,反应前铜、氢、氮、氧原子数目分别为1、4、4、12,反应后的生成物中铜、氢、氮、氧原子数目分别为1、4、2、8,根据反应前后原子种类、数目不变则2X分子中含有2个氮原子和4个氧原子,则每个X分子由1个氨原子和2个氧原子构成,则物质X的化学式为NO2。

 名校课堂系列答案
名校课堂系列答案【题目】我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn) ,它可用来制造电器零件及日用品。将30g稀盐酸分三次加入到10g 黄铜样品粉末中(不考虑黄铜中的其他杂质),每次充分反应后,测定本次生成氢气的质量,实验数据见下表:
次数 | 第一次 | 第二次 | 第三次 |
加入稀盐酸的质量(g) | 10 | 10 | 10 |
本次生成氢气的质量(g) | 0.04 | m | 0.02 |
请回答:
(1)工业上常用铜作电缆的内芯,是利用铜具有良好的____________性。
(2) m=____________。
(3)所用稀盐酸的溶质质量分数___________? (结果精确到0.1)