题目内容
【题目】现取含有氯化钠杂质的纯碱样品25g放入烧杯中,向烧杯中加入167g水使样品全部溶解,向烧杯中加入100g,氯化钙溶液,恰好完全反应,然后过滤,称得滤液的质量为272g,试计算:
(1)纯碱样品中氯化钠的质量分数_______.
(2)所得滤液中溶质的质量_______
【答案】15.2% 10%
【解析】
解:由质量守恒定律可知,生成的碳酸钙的质量为:25g+167g+100g-272g=20g
设恰好完全反应时参加反应的碳酸钠的质量为x,反应生成的氯化钠质量为y
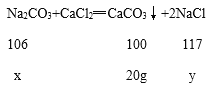
106:100=x:20g
x=21.2g
100:117=20g:y
y=23.4g
(1)则纯碱中氯化钠的质量分数为:![]() ×100%=15.2%;
×100%=15.2%;
(2)反应后所得滤液中溶质的质量分数是:![]() ×100%=10%
×100%=10%
答: (1)纯碱样品中氯化钠的质量分数为15.2%;
(2)所得滤液中溶质的质量10%。

练习册系列答案
相关题目