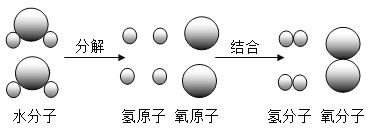
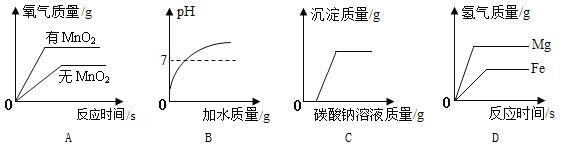
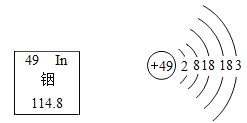��Ŀ����
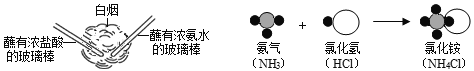
����Ŀ����ѧ������Ľ����ܲ��ɷ֡���ش���������⣺
��1�����ֽ�������ѹ�ɱ�Ƭ�����ϸ˿��˵����������_____�ԡ�
��2����Ԫ�������庬����ߵĽ���Ԫ�ء�����ȱ�ƻ�����_____��ѡ����ĸ����
AƶѪ ��B��������֢�� C��״���״�
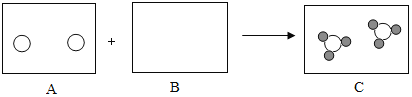
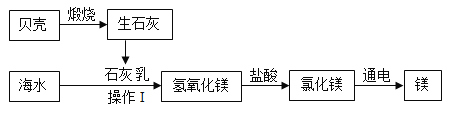
��3������Ӧ����㷺�Ľ�������ҵ�ϳ��ó������һ����̼�ڸ����������������÷�Ӧ�Ļ�ѧ����ʽΪ_____��
��4����ѧ����Xe��������ϳ��������ϲ���믣���ѧʽXePtF6�����ڸ�������Xe��FԪ�صĻ��ϼ۷ֱ���+1����1�����������ϲ���믵Ļ�ѧʽ�ϱ����Ԫ�صĻ��ϼ�_____��
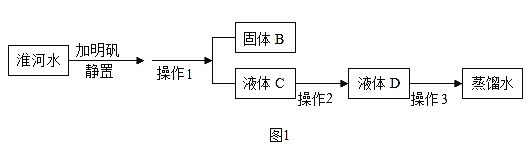
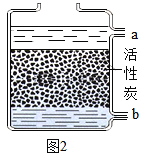
��5����ˮ���þ��˻����ˮ������ɷ���Ҫ��̼��þ��̼��ƣ�����ͨ������_____���������г�����һ�ֵ�ζƷ����ȥˮ����
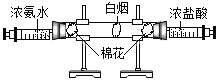
��6���ڹ�����Ҫ��ȥ����Ʒ��������⣬ͨ����ѡ��_____����һ�ּ��ɣ���Ϊ�������
���𰸡���չ B 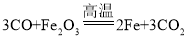
![]() ʳ�� ϡ����
ʳ�� ϡ����
��������
��1�����ֽ�������ѹ�ɱ�Ƭ�����ϸ˿��˵������������չ�ԣ�
��2������ȱ�ƻ�������������֢����ѡB��
��3�����������Ҫ�ɷ�������������������һ����̼�ڸ��µ������·�Ӧ�������Ͷ�����̼���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�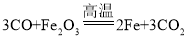 ��
��
��4�������ڻ������У��������ϼ۴�����Ϊ�㣬�責Ԫ�صĻ��ϼ�Ϊx��+1+x+����1����6��0�����x��+5��Ԫ�ػ��ϼ۵ı�ʾ�������ڻ�ѧʽ��Ԫ�ص��Ϸ��������ź����ֱ�ʾ�������ű�������ǰ�棬���������ϲ���믵Ļ�ѧʽ�ϱ����Ԫ�صĻ��ϼ�Ϊ��![]() ��
��
��5��ˮ���ɷ���Ҫ��̼��þ��̼��ƶ�����������ˮ�����ʣ��������ᷴӦ��������ʳ���ܳ�ȥˮ����
��6���������������ᷴӦ�����κ�ˮ��������Ҫ�ɷ�����������������ϡ������⡣

 ���źþ���Ԫ����ĩ��ϵ�д�
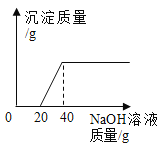
���źþ���Ԫ����ĩ��ϵ�д�����Ŀ��ij����С��ͬѧΪ�˲ⶨʯ��ʯ��̼��Ƶ�����������ȡij��ʯ��ʯ��Ʒ9.0g���ձ��У���50gϡ�����5�μ����ձ��У���ַ�Ӧ��![]() ���ʲ���ϡ���ᷴӦ
���ʲ���ϡ���ᷴӦ![]() �����ʣ������������¼���¡�
�����ʣ������������¼���¡�
���� | 1 | 2 | 3 | 4 | 5 |
����ϡ�������� | 10 | 10 | 10 | 10 | 10 |
ʣ��������� | 7.0 | 5.0 | 3.0 | 1.8 | X |
�����:
��1��X��ֵΪ______��
��2����ʯ��ʯ��Ʒ��̼��Ƶ���������Ϊ______��
��3������ϡ�������ʵ�����������![]() д���������
��������![]()