题目内容
【题目】如下图为几种固体的溶解度曲线,回答下列问题:
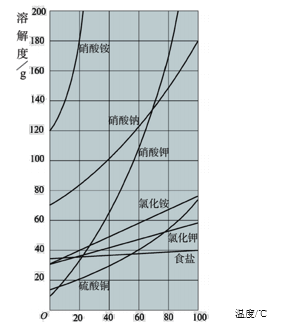
(1)CuSO4的溶解度约为20g时,其对应的温度是_______℃;若想使该饱和溶液转化为不饱和溶液,可采取的方法是______(写出一种即可),用此方法后,溶液的质量分数____(填“有”或“没有”)发生变化。
(2)80℃时,140g NaNO3溶于100g水形成的溶液 是_______溶液(填“饱和”或“不饱和”)。
(3)20℃时,NH4NO3溶液的溶质质量分数最大为___________(计算结果保留到0.1%)。
(4)若KNO3溶液中混有少量的NaCl杂质,可以采 取______方法获得较纯净的KNO3固体。
(5)60℃时分别将等质量的KNO3、NaCl、CuSO4 的 饱和溶液各500g恒温蒸发掉100g水,析出晶体
最多的是____。
(6)60℃时,10g NaCl和90g KNO3完全溶解于100g 蒸馏水中,冷却到30℃后,_________(“有”或“没有”)NaCl析出,有______________g KNO3结晶析出。
【答案】 20 加水 有 不饱和 64.3% 降温结晶 KNO3 没有 40
【解析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,根据溶解度的含义可以进行有关的分析与计算;②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。(1)由CuSO4的溶解度曲线可以查出,CuSO4的溶解度约为20g时,其对应的温度是20℃;若想使该饱和溶液转化为不饱和溶液,可采取的方法是加水,用此方法后,溶液的质量分数有发生变化(变小);(2)由NaNO3的溶解度曲线可以查出,在80℃时,NaNO3溶解度是150g,140gNaNO3溶于100g水形成的溶液是不饱和溶液;(3)由NH4NO3的溶解度曲线可以查出,20℃时,NH4NO3溶解度是180g,饱和溶液的溶质质量分数最大,为: ![]() ≈64.3%;(4)由溶解度曲线可知,由于KNO3的溶解度受温度的影响较大,NaCl的溶解度受温度的影响不大,若KNO3溶液中混有少量的NaCl杂质,可以采取降温结晶方法获得较纯净的KNO3固体;(5)60℃时分别将等质量的KNO3、NaCl、CuSO4的饱和溶液各500g恒温蒸发掉100g水,由于KNO3的溶解度最大,析出晶体最多的是KNO3;(6)由溶解度曲线可知,在30℃是氯化钠的溶解度是36.3g,KNO3的溶解度是50g,60℃时,10gNaCl和90gKNO3完全溶解于100g蒸馏水中,冷却到30℃后,没有NaCl析出,有KNO3结晶析出,质量为90g-50g=40g。
≈64.3%;(4)由溶解度曲线可知,由于KNO3的溶解度受温度的影响较大,NaCl的溶解度受温度的影响不大,若KNO3溶液中混有少量的NaCl杂质,可以采取降温结晶方法获得较纯净的KNO3固体;(5)60℃时分别将等质量的KNO3、NaCl、CuSO4的饱和溶液各500g恒温蒸发掉100g水,由于KNO3的溶解度最大,析出晶体最多的是KNO3;(6)由溶解度曲线可知,在30℃是氯化钠的溶解度是36.3g,KNO3的溶解度是50g,60℃时,10gNaCl和90gKNO3完全溶解于100g蒸馏水中,冷却到30℃后,没有NaCl析出,有KNO3结晶析出,质量为90g-50g=40g。

【题目】分类是学习化学的重要方法之一,初中学习中接触到下列物质:
A生铁 | B电解水负极得到的气体 | C冰水 | D氧化铝 |
E硝酸铵 | F洁净的空气 | G金刚石 | H硝酸钾 |
请按要求填写下列内容。
(1)其中属于纯净物的是_____(填序号)。
(2)标出氧化铝中铝元素的化合价_____。
(3)由原子构成的物质的是_____(填化学式,下同)。
(4)属于复合肥是_____。