题目内容
【题目】下列各组各有两种物质,它们的化学式和所属的物质类别都正确的一组是( )
物质1 | 物质2 | ||||||
名称 | 化学式 | 物质类别 | 名称 | 化学式 | 物质类别 | ||
A | 氮气 | N | 非金属单质 | 氧化亚铁 | Fe2O2 | 碱 | |
B | 碳酸氢钠 | NaHCO3 | 盐 | 硝酸 | HNO3 | 酸 | |
C | 硫酸钾 | K2SO4 | 盐 | 五氧化二磷 | P2O5 | 金属氧化物 | |
D | 锰 | Mm | 金属单质 | 氢氧化镁 | Mg(OH)2 | 碱 | |
A.A B.B C.C D.D
【答案】B
【解析】A、氮气的化学式为:N2,氧化亚铁的化学式为:FeO,属于金属氧化物而非碱(金属离子和氢氧根离子),故A错误;
B、物质名称和化学式及物质类别对应完全正确,故B正确;
C、五氧化二磷属于非金属氧化物,故C错误;
D、锰的元素符号是Mn,而非Mm,故D错误;
故选:B.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】在H、C、O、N四种元素中,选择一种或若干种用化学式填写下列空格:
(1)可用于灭火的气体 ;(2)相对分子质量最小的氧化物 ;
(3)一种可再生的液体燃料 ;(4)能支持动植物呼吸的一种单质 .
【题目】定量研究对于化学科学发展有重大作用,因此我们应该掌握好有关质量守恒定律的相关知识。
(1)在验证质量守恒定律时,下列A、B、C三个实验设计中,不能达到实验目的的是______(选填序号),理由是_______________。
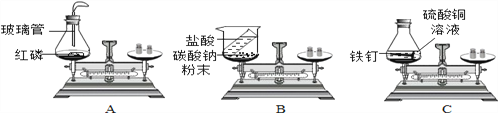
(2)从微观角度分析,解释反应中,质量守恒定律成立的原因是:_____。
(3)在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 | A | B | C | D |
反应前质量/g | 2 | 24.5 | 4 | 8 |
反应后质量/g | 16.9 | 0 | 13.6 | X |
表中X=______,该反应中D物质可能起了_________作用。容器内发生的反应的基本类型是_________。