题目内容
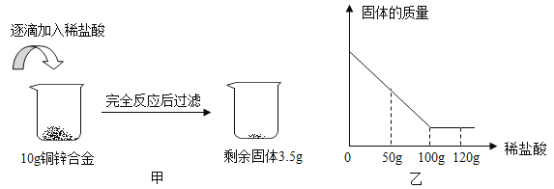
【题目】如图甲所示,向一定量的铜锌合金中,逐滴加入稀盐酸,反应过程中固体与稀盐酸的质量变化如图乙所示。请计算:
(1)铜锌合金中,铜的质量分数为_____。
(2)所用稀盐酸的溶质质量分数是多少_____?
【答案】35% 7.3%
【解析】
(1)铜的活动性位于金属活动性顺序中氢的后面,不能与酸反应生成氢气,所以铜锌合金中与稀盐酸反应的是锌,由图甲可知,完全反应后剩余的3.5g固体为铜,所以铜锌合金中,铜的质量分数为![]() ×100%=35%
×100%=35%
(2)由(1)可知,参加反应的锌的质量为10g3.5g=6.5g,由图可知,锌完全反应时消耗的稀盐酸的质量为100g
设所用稀盐酸的溶质质量分数是x
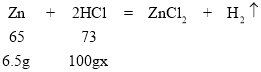
65:73= 6.5:100gx
x=7.3%
答:(1)铜锌合金中,铜的质分数为35%;
(2)所用稀盐酸的溶质质量分数是7.3%。

练习册系列答案
相关题目