题目内容
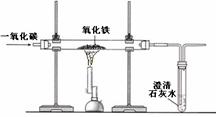
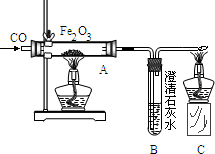 右图是一氧化碳还原氧化铁的实验装置图,下列有关该反应的说法正确的是
右图是一氧化碳还原氧化铁的实验装置图,下列有关该反应的说法正确的是
- A.当反应完成时可看到A中的红棕色粉末变成了银白色
- B.该实验中只能体现出一氧化碳一条化学性质
- C.实验开始时应先通一氧化碳再加热
- D.若要还原160g氧化铁,实际通入的一氧化碳为84g
C
分析:A、从CO还原氧化铁为铁考虑;
B、该实验中能体现出一氧化碳的还原性和可燃性;
C、从可燃性气体不纯加热有爆炸的危险考虑;
D、根据一氧化碳还原氧化铁的化学反应式计算判断.
解答:A、当反应完成时,A中的红棕色氧化铁被还原成黑色的铁,就是说A中的红棕色粉末变成了黑色,故错误;
B、从在A处表现的是还原性,在C处表现的是可燃性,故错误;
C、CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此,应先通CO排尽玻璃管中的空气,然后再加热.故正确;
D、根据化学反应式:Fe2O3+3CO 2Fe+3CO2↑计算可知还原160g氧化铁CO84g,因实验前还有先通入CO,所以实际用量要超过84g.故错误.
2Fe+3CO2↑计算可知还原160g氧化铁CO84g,因实验前还有先通入CO,所以实际用量要超过84g.故错误.
故选C
点评:本题考查了高炉炼铁的原理以及实验中的注意点(先通气体后加热,尾气处理)和实验现象(粉末由红变黑,石灰水变浑浊)
分析:A、从CO还原氧化铁为铁考虑;
B、该实验中能体现出一氧化碳的还原性和可燃性;
C、从可燃性气体不纯加热有爆炸的危险考虑;
D、根据一氧化碳还原氧化铁的化学反应式计算判断.
解答:A、当反应完成时,A中的红棕色氧化铁被还原成黑色的铁,就是说A中的红棕色粉末变成了黑色,故错误;
B、从在A处表现的是还原性,在C处表现的是可燃性,故错误;
C、CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此,应先通CO排尽玻璃管中的空气,然后再加热.故正确;
D、根据化学反应式:Fe2O3+3CO
 2Fe+3CO2↑计算可知还原160g氧化铁CO84g,因实验前还有先通入CO,所以实际用量要超过84g.故错误.
2Fe+3CO2↑计算可知还原160g氧化铁CO84g,因实验前还有先通入CO,所以实际用量要超过84g.故错误.故选C
点评:本题考查了高炉炼铁的原理以及实验中的注意点(先通气体后加热,尾气处理)和实验现象(粉末由红变黑,石灰水变浑浊)

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
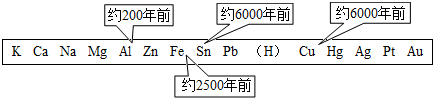

 (2010?白下区一模)煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
(2010?白下区一模)煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.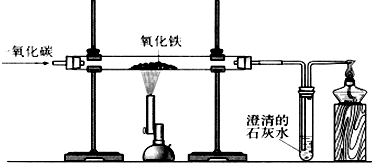


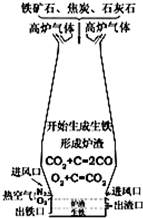
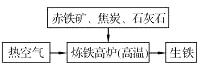 (1)右图是工业炼铁示意图。其中,焦炭的作用是燃烧提供能量和 ;写出有铁生成的化学方程式 。
(1)右图是工业炼铁示意图。其中,焦炭的作用是燃烧提供能量和 ;写出有铁生成的化学方程式 。