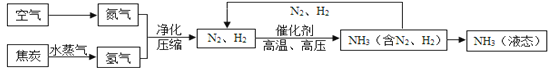
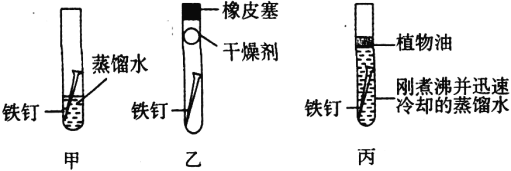
题目内容
【题目】(3分)回答下列问题:
(1)阅读下图包装说明,这袋化肥中氮元素的质量为 kg;碳酸氢铵的质量为 kg。(结果保留小数点后一位)

(2)欲将50kg10%的碳酸氢铵溶液稀释成1%的溶液,用于农作物的催肥,需加 kg水。
【答案】(1)8.4 47.4 (2)450
【解析】
试题分析:(1)根据标签,该化肥的含氮量为16.8%,那么氮元素的质量=50kg×16.8%=8.4kg;
碳酸氢铵中氮元素的质量分数=14/79 ×100%=17.7%
氮元素全部来自碳酸氢铵,故碳酸氢铵的质量=8.4kg÷17.7%= 47.4kg
(2)溶液稀释前后溶质的质量不变,设稀释后溶液的质量为,
50kg×10%=1%x
X=500kg
加入水的质量=500kg-50kg=450kg

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案【题目】(8分)常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
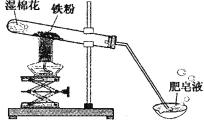
(1)试管尾部放一团湿棉花的目的是_______________。
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是______________。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_____________
【实验探究】
实验操作 | 实验现象及结论 |
【实验结论】铁和水蒸气反应的化学方程式为_________________________________。
【反思与交流】该黑色固体不可能是Fe2O3,理由是___________________________。