题目内容
(2011?清远)学习了CO2的有关知识之后,同学们查阅资料发现Mg能在CO2中燃烧:2Mg+CO2 2MgO+C,所以镁着火不能用CO2来灭火.但没有找到有关钠能否与CO2反应的介绍.于是同学们展开钠着火能否用CO2来灭火的探究.
2MgO+C,所以镁着火不能用CO2来灭火.但没有找到有关钠能否与CO2反应的介绍.于是同学们展开钠着火能否用CO2来灭火的探究.(一)【提出猜想】
钠能发生类似于CO2与镁的反应,可能的化学方程式为:______ 2Na2O+C
【答案】分析:【提出猜想】钠能发生类似于CO2与镁的反应,用类比的方法可书写其发生的化学方程式;
【实验】根据资料,同学们认为钠在CO2中燃烧的产物应该与Mg在CO2中燃烧的产物情况有所不同,并对产物提出几种猜想;通过理论分析,猜想③(填序号)肯定是错误的,理由是:根据质量守恒定律可知.
【验证猜想】
由操作和现象,得出结论;或由操作和结论,推测现象;或由现象和结论,推测操作.了解在步骤(2)中BaCl2溶液为什么要加入至过量的原因.
在步骤(3)中也可以通过加入酸碱指示剂或能与OH-反应生成沉淀的可溶性物质.
【结论】由猜想得结论.
解答:解:【提出猜想】钠能发生类似于CO2与镁的反应,故可用类比的方法书写其发生的化学方程式为:
4Na+CO2 2Na2O+C.
2Na2O+C.
【实验】将燃着的钠伸入装有CO2的集气瓶中,钠能在CO2中继续燃烧.
进一步查阅资料得知:①Na2O是白色固体,能与CO2反应生成Na2CO3,与H2O反应生成NaOH.②Ba(OH)2溶于水而BaCO3不溶于水.③Na2CO3的存在会干扰NaOH的检测.
基于以上资料,同学们认为钠在CO2中燃烧的产物应该与Mg在CO2中燃烧的产物情况有所不同,并对产物提出了以下几种猜想:①Na2O、C ②Na2CO3、C ③NaOH、C ④Na2O、Na2CO3、C
通过理论分析,猜想:③(填序号)肯定是错误的,理由是:NaOH中有氢元素而反应物中没有氢元素,根据质量守恒定律可知③错误.
【验证猜想】由操作和现象,得出结论;或由操作和结论,推测现象;或由现象和结论,推测操作:故
在步骤(2)中BaCl2溶液为什么要加入至过量:完全除去Na2CO3,以免Na2CO3干扰NaOH的检验.
在步骤(3)中也可以通过加入:酚酞(或紫色石蕊试液、或能与OH-反应生成沉淀的可溶性物质)试剂的方法进行检验.
【结论】猜想④(填序号)正确.
故答为:(一)、4Na+CO2 2Na2O+C;
2Na2O+C;
(二)、2、②Na2CO3;3、③;NaOH中有氢元素而反应物中没有氢元素,根据质量守恒定律可知③错误;
(三)答案见表格
1、完全除去Na2CO3,以免Na2CO3干扰NaOH的检验;
2、酚酞(或紫色石蕊试液、或能与OH-反应生成沉淀的可溶性物质);
四、④
点评:掌握质量守恒定律的也是守恒的思想处理问题;了解物质的鉴别与推断的方法.
【实验】根据资料,同学们认为钠在CO2中燃烧的产物应该与Mg在CO2中燃烧的产物情况有所不同,并对产物提出几种猜想;通过理论分析,猜想③(填序号)肯定是错误的,理由是:根据质量守恒定律可知.
【验证猜想】
由操作和现象,得出结论;或由操作和结论,推测现象;或由现象和结论,推测操作.了解在步骤(2)中BaCl2溶液为什么要加入至过量的原因.
在步骤(3)中也可以通过加入酸碱指示剂或能与OH-反应生成沉淀的可溶性物质.
【结论】由猜想得结论.
解答:解:【提出猜想】钠能发生类似于CO2与镁的反应,故可用类比的方法书写其发生的化学方程式为:
4Na+CO2
 2Na2O+C.
2Na2O+C.【实验】将燃着的钠伸入装有CO2的集气瓶中,钠能在CO2中继续燃烧.
进一步查阅资料得知:①Na2O是白色固体,能与CO2反应生成Na2CO3,与H2O反应生成NaOH.②Ba(OH)2溶于水而BaCO3不溶于水.③Na2CO3的存在会干扰NaOH的检测.
基于以上资料,同学们认为钠在CO2中燃烧的产物应该与Mg在CO2中燃烧的产物情况有所不同,并对产物提出了以下几种猜想:①Na2O、C ②Na2CO3、C ③NaOH、C ④Na2O、Na2CO3、C
通过理论分析,猜想:③(填序号)肯定是错误的,理由是:NaOH中有氢元素而反应物中没有氢元素,根据质量守恒定律可知③错误.
【验证猜想】由操作和现象,得出结论;或由操作和结论,推测现象;或由现象和结论,推测操作:故
| 步骤 | 实验操作 | 主要实验现象 | 结论(燃烧产物判断) |
| (1) | 将产物溶于适量水中 | 部分溶解,试管 底部有黑色固体 | 燃烧产物中肯定有C(炭) |
| (2) | 取(1)所得少量上层清液,加入过量的BaCl2溶液 | 有白色沉淀生成 | 燃烧产物中肯定有Na2CO3 |
| (3) | 取(2)所得少量上层清液,加入 CuSO4(或CuCl2)溶液溶液 | 有蓝色沉淀生成 | 燃烧产物中肯定有 Na2O |
在步骤(3)中也可以通过加入:酚酞(或紫色石蕊试液、或能与OH-反应生成沉淀的可溶性物质)试剂的方法进行检验.
【结论】猜想④(填序号)正确.
故答为:(一)、4Na+CO2
 2Na2O+C;
2Na2O+C;(二)、2、②Na2CO3;3、③;NaOH中有氢元素而反应物中没有氢元素,根据质量守恒定律可知③错误;
(三)答案见表格
| 步骤 | 实验操作 | 主要实验现象 | 结论(燃烧产物判断) |
| (1) | 将产物溶于适量水中 | 部分溶解,试管 底部有黑色固体 | 燃烧产物中肯定有C(碳) |
| (2) | 取(1)所得少量上层清液,加入过量的BaCl2溶液 | 有白色沉淀生成 | 燃烧产物中肯定有Na2CO3 |
| (3) | 取(2)所得少量上层清液,加入 CuSO4(或CuCl2)溶液溶液 | 有蓝色沉淀生成 | 燃烧产物中肯定有 Na2O |
2、酚酞(或紫色石蕊试液、或能与OH-反应生成沉淀的可溶性物质);
四、④
点评:掌握质量守恒定律的也是守恒的思想处理问题;了解物质的鉴别与推断的方法.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
(2011?珠海)学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量好化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后______.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
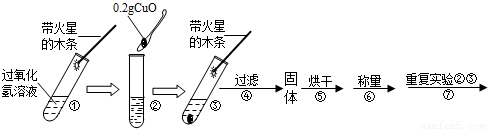
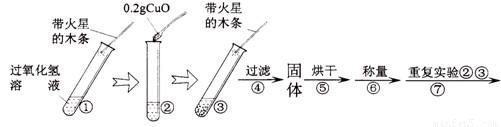
(1)填写下表:
(2)步骤①的目的是______.
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、______.
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为______ 2H2O+O2↑
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量好化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后______.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:


(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| ______ 带火星的木条复燃. | ______ | 溶液中有气泡放出, ______ | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、______.
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为______ 2H2O+O2↑