题目内容
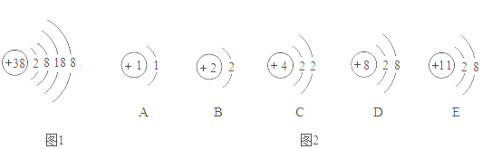
【题目】为试验稀H2SO4的化学性质,同学们做了如下实验:

(1)五个试管中,没有明显现象的是_____。
(2)写出试管B中发生反应的化学方程式_____。
同学们将实验后的所有物质倒入同一烧杯中,后续实验及现象如图:
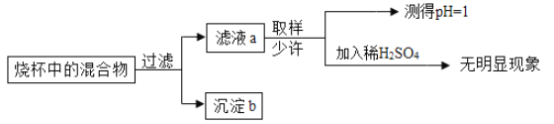
(3)沉淀b的成分有_____。
(4)溶液a中一定含有的溶质_____。
(5)排放溶液a前需要处理,可以加入适量的下列物质中的_____(注:Cu2+、Ba2+有毒)。
A NaOH
B BaCO3
C Ca(OH)2
D 铁粉
【答案】A CuO+H2SO4═CuSO4+H2O 铜、硫酸钡 硫酸铜、硫酸钠、硝酸 AC
【解析】
(1)五个试管中,没有明显现象的是A,这是因为铜不能和稀硫酸反应,B中固体溶解,溶液变蓝色,C中溶液由红色变成无色,D中产生气泡,E中产生白色沉淀。
故填:A。
(2)试管B中氧化铜和稀硫酸反应生成硫酸铜和水,发生反应的化学方程式:CuO+H2SO4═CuSO4+H2O。
故填:CuO+H2SO4═CuSO4+H2O。
(3)测定溶液的pH=1,说明溶液显酸性,加入稀硫酸无明显现象,说明硝酸钡完全反应,因此沉淀b的成分有铜、硫酸钡。
故填:铜、硫酸钡。
(4)溶液a中一定含有的溶质:氧化铜和稀硫酸反应生成的硫酸铜、反应生成的硫酸钠和硝酸。
故填:硫酸铜、硫酸钠、硝酸。
(5)A、NaOH能和硫酸铜、硝酸反应,因此可以加入氢氧化钠;
B、BaCO3能和硝酸反应生成硝酸钡,因此不能加入碳酸钡;
C、Ca(OH)2能和硫酸铜、硝酸反应,因此可以加入氢氧化钙;
D、铁粉能和硫酸铜、硝酸反应,铁和硝酸反应生成氮氧化物,污染环境,因此不能加入铁粉。
故填:AC。

 名校课堂系列答案
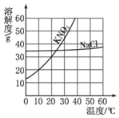
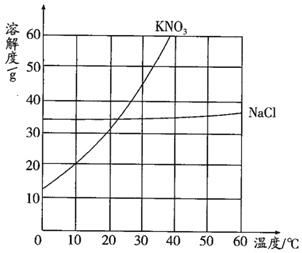
名校课堂系列答案【题目】根据给出的KNO3和NaC1两种物质的溶解度表及溶解度曲线,回答问题。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
(1)在40℃时,NaC1的溶解度为_____。
(2)除去KNO3中含有的少量NaC1,先将混合物溶于热水配成饱和溶液,然后经过_____过滤,即可得到较纯的KNO3。
(3)20℃,将40gKNO3放入100g水中充分搅拌,再升温到60℃,下列说法正确的是_____
A 得到饱和溶液 B 溶剂的质量不变
C KNO3的溶解度减小 D 溶质的质量分数增大。
【题目】生理盐水是0.9%的氯化钠水溶液,因为它的渗透压值和正常人的血浆、组织液都是大致一样的,所以可以用作补液以及其他医疗用途。已知氯化钠在不同温度时的溶解度如下表所示:
温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 |
溶解度/g | 35.7 | 35.8 | 36.0 | 36.6 | 37.3 | 38.4 |
下列说法中不正确的是( )
A. 氯化钠的溶解度随着温度的升高而增大
B. 20℃时的生理盐水是氯化钠的不饱和溶液
C. 将80℃时的氯化钠的饱和溶液冷却至20℃,有结晶现象
D. 40℃时,100g氯化钠的饱和溶液中氯化钠的质量为36.6g