题目内容
【题目】下图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。
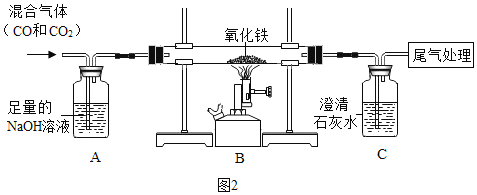
(1)B装置玻璃管里可观察到的现象是_____。
(2)实验结束后,若要确定A装置溶液中溶质的成分,请设计合理的实验方案,简要写出实验步骤、现象和结论。_____(提示:Na2CO3,溶液呈碱性)
【答案】红棕色粉末逐渐变黑 取溶液少许,加入足量的氯化钙溶液,然后向清液中加入酚酞试液,若变成红色,说明含有氢氧化钠,否则不含有氢氧化钠
【解析】
(1)用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,硬质玻璃管中变化的现象红棕色粉末逐渐变黑;
(2)实验结束后,若要确定A装置溶液中溶质的成分,其中一定含有碳酸钠,应验证是否含有氢氧化钠,应先除去碳酸钠,所以验证,请设计合理的实验方案是:取溶液少许,加入足量的氯化钙溶液,然后向清液中加入酚酞试液,若变成红色,说明含有氢氧化钠,否则不含有氢氧化钠。

【题目】某学校化学活动小组的同学对碳酸钠与稀盐酸的反应进行了下列探究:
[探究一]向放有一支燃着的蜡烛的烧杯中加适量碳酸钠和稀盐酸(如图1所示):
(1)烧杯中看到的现象是:______________,说明二氧化碳具有的化学性质是:___________ 。
(2)碳酸钠与稀盐酸反应产生的气体具有的另一个用途是____________ 。
[探究二]碳酸钠与稀盐酸反应后剩余溶液的成分探究(假设二氧化碳已完全放出,杂质溶于水,不参加反应且呈中性)。甲、乙两同学分析认为剩余溶液中一定含有氯化钠,可能有盐酸或碳酸钠。为验证是否含有盐酸,他们采用了不同方法进行实验,得到了相同的结论。
查找资料:氯化钠溶液呈中性
实验操作 | 实验现象 | 结论 | |
甲 | 取样于试管中,滴加__________试液 | 试液变红 | 有盐酸 |
乙 | 取样于试管中,逐滴滴加碳酸钠溶液 | ______________ |
[探究三]测定所用稀盐酸的溶质质量分数?[实验原理]通过测定足量碳酸钠样品与一定质量的稀盐酸反应生成二氧化碳的体积来计算稀盐酸的溶质质量分数。
[实验设计]小伍称取一定质量的样品,按如图2装置进行实验(已知该装置气密性良好,水准管高度可以上下调节,量气管是带有刻度的仪器)。
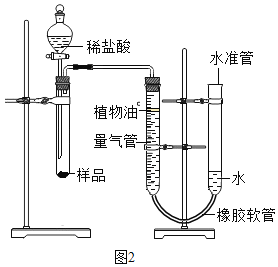
[反思与评价](1)在实验中,若没有植物油,测定结果会________(填“偏大”、“偏小”或“不变”)。
(2)操作中,下列情况不影响测定结果的是___________(填字母).
A实验前试管中有空气 B实验中水准管口有水溢出
C读数时量气管和水准管液面不相平 D实验后生成的气体在试管中仍有滞留