题目内容
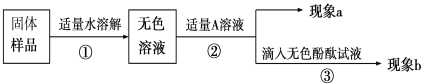
【题目】根据酸的化学性质回答下列问题:

(1)酸溶液有相似化学性质的原因是溶液中都含有________(填粒子符号)。
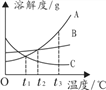
(2)图中X代表一类物质,X属于____________(填物质类别)。
(3)性质③发生的反应属于_________反应。
(4)写出符合性质④的一道化学反应方程式____________。
【答案】H+ 金属氧化物 复分解(或中和) HCl + AgNO3=AgCl↓+ HNO3
【解析】
酸的化学性质:①能和酸碱指示剂反应。②酸和金属反应生成盐和氢气。③酸和金属氧化物反应生成盐和水。④酸和碱反应生成盐和水。⑤酸和某些盐反应生成新酸和新盐。
(1)酸溶液具有相似的化学性质是都能在水溶液中电离出氢离子。故答案为:H+;
(2)根据分析可知,能和酸反应生成盐和水的是金属氧化物或碱。则X为金属氧化物。故答案为:金属氧化物;
(3)③描述的是酸和碱反应生成盐和水。该反应属于复分解反应,也属于中和反应。故答案为:复分解(或中和);
(4)酸和某些盐反应生成新酸和新盐。则该反应可能是稀盐酸和硝酸银反应生成硝酸和氯化银沉淀。故答案为:HCl+AgNO3=AgCl↓+HNO3(答案合理即可)。

【题目】下列实验中,现象与结论对应关系正确的是
A | B | C | D | |
图示 |
|
|
|
|
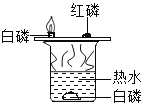
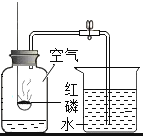
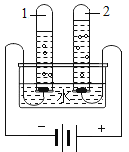
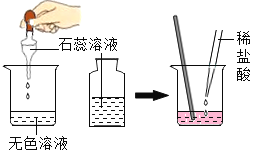
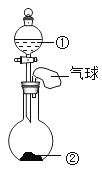
现象 | 铜片上白磷燃烧红磷不燃烧,水中白磷不燃烧 | 冷却后,打开弹簧夹,水被吸入瓶内,瓶内水面上升约 1/5 | 试管 1 中的气体燃烧,产生淡蓝色火焰,试管 2 中的气体能使带火星的木条复燃 | 滴有石蕊的溶液呈蓝色,加入稀盐酸后蓝色变为红色 |
结论 | 水中白磷不燃烧,因为没有达到着火点 | 氧气约占空气质量的 1/5 | 水是由氧气和氢气组成的 | 反应后的溶液中一定不含碱性物质 |
A.AB.BC.CD.D
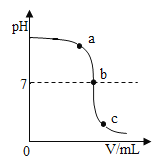
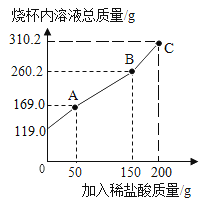
【题目】为测定久置于空气中的氢氧化钠样品的变质程度,某化学活动小组称取该固体样品6.5g放入锥形瓶中,加水溶解,配成50g溶液,再向锥形瓶中滴加稀硫酸,反应过程中产生气体质量的部分实验数据和锥形瓶中溶液质量变化的图象如表所示:
加入稀硫酸的质量/g | 40 | 65 | 75 |
产生气体的质量/g | 1.1 | 2.2 | 2.2 |
(1)6.5g样品与稀硫酸完全反应产生气体的质量是________g。
(2)6.5g样品中碳酸钠的质量分数是________。(结果精确至0.1%)
(3)以上三次的实验数据中,只有一次加入的稀硫酸与锥形瓶中溶液的溶质恰好完全反应。
①如图图象中a的数值是________。
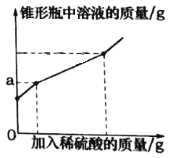
②求该实验中所用稀硫酸的溶质质量分数____。(写出计算过程)