题目内容
【题目】牙膏摩擦剂的类型很多,如CaCO3、SiO2或它们的混合物.某兴趣小组对某品牌牙膏摩擦剂的成分进行了如下探究. 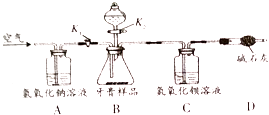
(1)【提出问题1】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应;碱石灰主要成分为生石灰与氢氧化钠.
【实验方案】取少量牙膏于试管中,加入适量的稀盐酸,出现气泡,将气体通入澄清石灰水,石灰水变浑浊,证明摩擦剂中含有(填离子符号);石灰水变浑浊的化学方程式为
(2)【实验装置】
①连接好装置后,首先进行的操作是 .
②在B装置中加入牙膏样品5g;
③K1 , K2(填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至B中无气泡产生时,停止滴加盐酸;
④打开K1 , 关闭K2 , 缓缓鼓入空气,至C中 .
⑤将C装置中的固液混合物过滤、洗涤、烘干后称量其质量为1.97g.(已知此品牌牙膏中的其他成分不和盐酸反应,装置内试剂均足量且充分反应.)
(3)【实验分析及数据处理】
①若没有A装置,则实验测定结果将 . (填“偏大”、“偏小”或“不变”)
②D装置的作用是 .
③根据上面数据计算,牙膏样品中碳酸钙的质量分数是 .
【答案】
(1)CO32﹣;Ca(OH)2+CO2=CaCO3↓+H2O
(2)检查装置的气密性;关闭;打开;不再产生沉淀
(3)偏大;防止空气中的二氧化碳进入装置C中;20%
【解析】解:【实验方案】
将气体通入澄清石灰水,石灰水变浑浊,说明该气体是二氧化碳,证明摩擦剂中含有碳酸钙,碳酸钙中含有碳酸根离子,碳酸根离子可以表示为CO32﹣;
二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
【提出问题2】该牙膏中CaCO3的质量分数是多少?
【实验步骤】
①连接好装置,首先进行的操作是检查装置的气密性;
③关闭K1 , 打开K2 , 然后向牙膏样品中滴入质量分数为10%的盐酸,至B中无气泡产生时,停止滴加盐酸;
④打开K1 , 关闭K2 , 缓缓鼓入空气,至C中不再产生沉淀;
【实验分析及数据处理】
①若没有A装置,则空气中的二氧化碳能够被氢氧化钡溶液吸收,从而导致测定结果偏大;
②D装置的作用是防止空气中的二氧化碳进入装置C中;
③设碳酸钙的质量为x,
由CaCO3+2HCl═CaCl2+H2O+CO2↑,Ba(OH)2+CO2═BaCO3↓+H2O可知,
CaCO3~BaCO3↓,
CaCO3~BaCO3↓,
100 197
x 1.97g![]()
x=1g,
牙膏样品中碳酸钙的质量分数为: ![]() ×100%=20%.
×100%=20%.
故答案为:
【实验方案】CO32﹣;Ca(OH)2+CO2=CaCO3↓+H2O;
【实验装置】
②检查装置的气密性;
③关闭;打开;
④不再产生沉淀;
【实验分析及数据处理】
①偏大;
②防止空气中的二氧化碳进入装置C中;
③20%.
【实验方案】碳酸钙能够稀盐酸反应生成氯化钙、水和二氧化碳,二氧化碳能使澄清石灰水变浑浊;
【实验步骤】凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
二氧化碳能和氢氧化钡反应生成白色沉淀碳酸钡和水;
氢氧化钠溶液能够吸收空气中的二氧化碳;
碱石灰能够吸收水和二氧化碳.

 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案