题目内容
两种铁的氧化物,其质量分别为0.400g和0.435g,使它们在高温条件下分别与一氧化碳反应,再把生成的二氧化碳全部通人足量的石灰水中,都得到了0.75g沉淀.则这两种氧化物分别是( )A.FeO和Fe2O3
B.FeO和Fe3O4
C.Fe2O3和Fe3O4
D.Fe3O4和Fe2O3
【答案】分析:由题意可知,铁的氧化物在高温条件下与一氧化碳反应,生成的二氧化碳与足量的石灰水反应,反应是分步进行的,根据反应的方程式,找出反应的关系式,再利用关系式进行计算,判断出氧化物.
解答:解:设铁的是氧化物是FexOy
由FexOy+yCO XFe+yCO2 CO2+Ca(OH)2═CaCO3↓+2H2O
XFe+yCO2 CO2+Ca(OH)2═CaCO3↓+2H2O
得出:FexOy~yCaCO3
当铁的氧化物是0.400g时
则 FexOy~yCaCO3
56x+16y 100y
0.4000克 0.75g
 =
=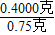 解得:
解得: =
=
所以 铁的氧化物是Fe2O3.
当铁的氧化物是0.435g时
则FexOy~yCaCO3
56x+16y 100y
0.435克 0.75g
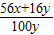 =
=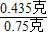 解得:
解得: =
=
所以 铁的氧化物是 Fe3O4,所以,C正确,A、B、D错误.
故选C.
点评:本题综合性较强,难度较大.解题的方法可用关系法进行解题,对于有些分步多步反应的化学方程式的计算,可以根据化学方程式找出关系式,利用关系式进行计算比较简便.
解答:解:设铁的是氧化物是FexOy
由FexOy+yCO
 XFe+yCO2 CO2+Ca(OH)2═CaCO3↓+2H2O
XFe+yCO2 CO2+Ca(OH)2═CaCO3↓+2H2O得出:FexOy~yCaCO3
当铁的氧化物是0.400g时
则 FexOy~yCaCO3
56x+16y 100y
0.4000克 0.75g
 =
=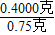 解得:
解得: =
=
所以 铁的氧化物是Fe2O3.
当铁的氧化物是0.435g时
则FexOy~yCaCO3
56x+16y 100y
0.435克 0.75g
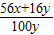 =
=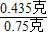 解得:
解得: =
=
所以 铁的氧化物是 Fe3O4,所以,C正确,A、B、D错误.
故选C.
点评:本题综合性较强,难度较大.解题的方法可用关系法进行解题,对于有些分步多步反应的化学方程式的计算,可以根据化学方程式找出关系式,利用关系式进行计算比较简便.

练习册系列答案
相关题目
两种铁的氧化物,其质量分别为0.400g和0.435g,使它们在高温条件下分别与一氧化碳反应,再把生成的二氧化碳全部通人足量的石灰水中,都得到了0.75g沉淀.则这两种氧化物分别是( )
| A、FeO和Fe2O3 | B、FeO和Fe3O4 | C、Fe2O3和Fe3O4 | D、Fe3O4和Fe2O3 |
有两种铁的氧化物X,Y,质量分别是0.4g与0.435g,在加热的条件下分别用CO还原成铁单质,把各自生成的CO2分别通入足量澄清石灰水中,都得到0.75g沉淀,则X、Y的分子式为( )
| A、FeO、Fe2O3 | B、Fe2O3、Fe3O4 | C、FeO、Fe3O4 | D、Fe3O4、Fe2O3 |