题目内容
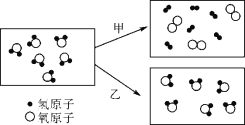
【题目】某工厂产生的铜屑中含有少量铁屑,现要回收利用其中的铜,需除去其中的铁屑,张山同学设计了甲、乙两个实验方案:
![]()
(1)以上两个实验方案中,从回收利用率的角度考虑,你愿意选择______________。
(2)两个方案中都有过滤操作,该操作中必须用到的玻璃仪器有______________。
(3)写出两个实验方案中有关反应的化学方程式:
方案甲:______________;方案乙:______________。
(4)你能否再设计一个不同原理的方案?写出你的答案:____________。
【答案】甲烧杯、漏斗、玻璃棒Fe+CuSO4===FeSO4+CuFe+H2SO4===FeSO4+H2↑用磁铁吸引
【解析】
(1)由于铁和硫酸铜溶液反应时还会生成一部分铜,因此在甲方案中得到的铜要多一些,因此应该选择甲;
(2)在过滤操作中一定会用到漏斗、烧杯、玻璃棒、铁架台、滤纸等,其中的玻璃仪器有漏斗、烧杯、玻璃棒;
(3)由于方案甲是铁和硫酸铜反应,而方案乙是铁和稀硫酸反应,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;Fe+H2SO4═FeSO4+H2↑;
(4)由于铁具有磁性,因此能被磁铁吸引,因此实验方案是:利用磁铁吸引。

练习册系列答案
相关题目