题目内容
【题目】水是生命之源,请回答下列问题。
(1)在水的净化过程中常加入明矾,明矾的作用是_____。
(2)制蒸馏水时,在蒸馏烧瓶中加入沸石(或碎瓷片),沸石(或碎瓷片)的作用是_____。
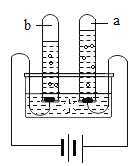
(3)电解水通电前,加入酚酞溶液,溶液呈无色,通电一段时间后,a试管中收集到的气体是_____,与b试管收集气体体积比是_____,b试管中的水溶液呈_____色,说明b试管中溶液pH_____7(填“>”、“<”或“=”)。
【答案】吸附悬浮的杂质 防止液体暴沸 氧气(或O2) 1:2 红 >
【解析】
(1)明矾溶于水后形成胶状物能吸附悬浮的杂质,使杂质沉降来达到净水的目的;
(2)实验中加入的沸石(或碎瓷片)的作用是防止液体暴沸;
(3)电解水时“正氧负氢,氢二氧一”,a试管连接正极,收集到的气体为氧气,与b试管收集气体体积比是1:2;水中加入了酚酞,实验过程中b试管溶液变红,说明溶液呈碱性,pH>7;
故答案为:(1)吸附悬浮的杂质;(2)防止液体暴沸;(3)氧气(或O2);1:2;红;>。

 名校课堂系列答案
名校课堂系列答案【题目】某化学兴趣小组在学习酸碱中和反应实验时,进行了如下探究:
I探究酸和碱能否发生反应
甲同学向盛有少量KOH溶液的试管中滴入几滴无色酚酞试液,振荡,继续加入稀盐酸,观察到溶液由_______色变成无色。甲同学得出结论:酸和碱能发生反应。
请写出稀盐酸和氢氧化钾溶液反应的化学方程式_____________。
Ⅱ探究酸和碱反应后溶液中溶质的成分
乙同学对探究I中甲同学实验后的无色溶液展开探究
(提出问题)试管中无色溶液的溶质除了酚酞还有什么?
(提出猜想)(1)KCl;(2)KCl和__________(填化学式)。
(设计实验)
方案 | 实验操作 | 实验现象及方程式 | 实验结论 |
方案1 | 试管中加入少量碳酸钠,然后加入过量甲同学实验后的无色溶液 | 可观察到溶液中有_______产生,化学反应方程式为________。 | 猜想(2)成立 |
方案2 | 用玻璃棒蘸取少量反应后的溶液滴在PH试纸上 | pH________7(填“>“<”或“=”) | |
方案3 | 取少量实验后的无色溶液于试管中,然后慢慢加NaOH溶液,并不断振荡试管 | 开始无明显现象,过一会发现_______。 |
(发散思维)
为了验证猜想(2)成立,你认为还可以选择的物质是_________(填选项)。
A二氧化碳 B锌粒 C氧化铜 D紫色石蕊试液
【题目】已知:CO2和SO2既有相似也有差异性。请回答相关问题:
气体 | CO2 | SO2 | |
制剂 | 石灰石与盐酸 | Na2SO3与70%硫酸 | |
相似性 | 溶解性 | 能溶于水 | 易溶于水 |
与澄清石灰水反应 | 二者都产生白色浑浊 | ||
差异性 | 与KMnO4溶液 | 不反应 | 气体被吸收,溶液逐渐褪色 |
(1)化石燃料燃烧气体产物中有CO2和SO2等物质,其中SO2是形成_______(填一污染名称)的主要物质。
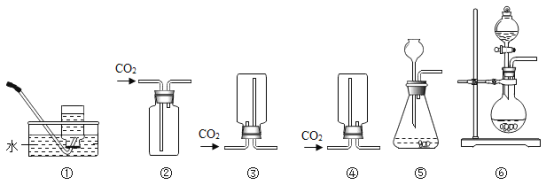
(2)实验室制取CO2的化学方程式是________,可用于收集CO2的装置是_______(选填下图序号)。
(3)将收集满SO2的试管倒扣在水中观察到的现象是_______。
(4)结合已知信息,请你设计实验证明化石燃料燃烧的气体产物中有CO2(写出操作、试剂、现象、结论)。________
(5)二氧化碳是一种宝贵的碳氧资源。一定条件下,二氧化碳转变成燃料甲醇(CH3OH)的化学式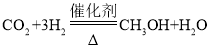 。若生产64t甲醇,则可回收二氧化碳多少吨?_____
。若生产64t甲醇,则可回收二氧化碳多少吨?_____
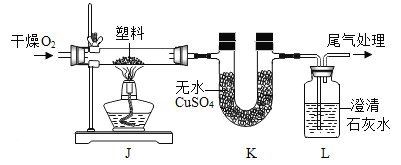
【题目】(1)定性检测(已知:无水CuSO4遇水变蓝色)
实验操作 | 实验现象 | 结论 |
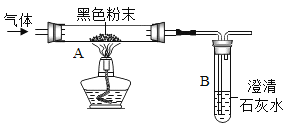
连接上图所示装置,_____,装入试剂,一段时间后,点燃J处酒精灯。 | 装置K中无水CuSO4_____色; | 塑料燃烧产物中有H2O |
装置L中澄清石灰水变浑浊。 | 塑料燃烧产物中有_____ |
由上述实验可知,该塑料一定含有的元素是_____(填元素符)。
(2)定量测定
为进一步确定组成,将2.8g该塑料在足量O2中完全燃烧,共产生了8.8gCO2和3.6gH2O,依据质量守恒定律,可判断该塑料_____(填“含有”或“不含”)除上述④中结论之外的元素。