题目内容
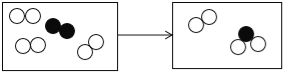
【题目】图中广口瓶里分别装入下列各组中的气体,滴管分别滴入各组中的液体时,玻璃管下端所系的气球能够鼓起来的是
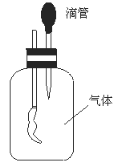
A.氢气、浓硫酸B.氮气、苛性钠溶液
C.HCl、水D.CO2、烧碱溶液
【答案】CD
【解析】考点定位分析:本题的考点是碱的化学性质,二氧化碳的化学性质,氢气的化学性质与燃烧实验。
解答过程分析:结合物理知识,套在玻璃管下端的小气球鼓起来,说明瓶中的压强减小,可能是两种物质相互作用吸热,也可能是气体被液体吸收,这两种情况都会导致锥形瓶中出现的实验现象,根据物质的间的反应规律判断分析,即可得出答案。
A、氢气和浓硫酸不反应,故瓶内气压不发生改变,此项错误;
B、氮气和苛性钠溶液不反应,瓶内气压不变,此项错误;
C、氯化氢易溶于水,使瓶内气压减小,气球膨胀,此项正确;
D、烧碱溶液能吸收二氧化碳气体,瓶内气压减小,此项正确。故选CD
试题总结评价:本题主要考查了如何根据实验现象判断物质之间能否反应方面的内容。解答本题要充分理解物质之间相互作用时的实验现象方面的知识,只有这样才能对相关方面的问题做出正确的判断。

 口算题天天练系列答案
口算题天天练系列答案【题目】某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据见下表。制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾不饱和溶液100g。

加热时间/min | 0 | t1 | t2 | t3 |
固体质量/g | 28.0 | 23.2 | 18.4 | 18.4 |
(1)共制得氧气 g。
(2)计算所得氯化钾溶液的溶质质量分数。
【题目】将一定量的苯(C6H6)和氧气置于一个完全密闭的容器中引燃,反应后生成二氧化碳、水和一种未知物X.测得反应前后各物质的质量如表:
物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 6.6 | 2.7 | m |
下列判断不正确的是( )
A. 表中m的值为4.2
B. 物质X由碳、氧元素组成
C. 物质X由碳、氢元素组成
D. 生产二氧化碳和水的分子个数比为2:1