题目内容
【题目】向硝酸铜、硝酸锌的混合液中加入一定量的铁粉充分反应后过滤,向滤渣中加稀硫酸有气体生成,则滤出的固体中有( )
A.Cu Zn
B.Cu Zn Fe
C.Zn Fe
D.Cu Fe
【答案】D
【解析】解:若向滤渣中加入稀硫酸,看到有气泡冒出,说明滤渣中含有铁粉,可判断混合溶液中硝酸铜已完全反应,则滤渣中一定含有Cu、Fe,一定无Zn. 故选:D.
【考点精析】本题主要考查了金属材料的选择依据的相关知识点,需要掌握黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属才能正确解答此题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
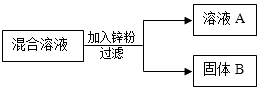
【题目】某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了右图实验,对固体B的成分进行了分析和实验探究. 【提出问题】固体B中的成分可能有哪些?
(1)【作出猜想】甲同学:只有Ag 乙同学:Zn、Ag
丙同学:Cu、Ag
请写出你的一种猜想
(2)【表达交流】写出甲同学猜想的理由
(3)【反思评价】请你评价乙同学的猜想
(4)【实验探究】想证明自己的猜想正确
实验步骤 | 现象 | 由此确定固体B的成分写出反应的化学方程式 |
取少量固体B,滴加 | 有气泡产生 |
在得出固体B的成分后,也确定了液体A的成分,液体A中含有的物质有(化学式)