题目内容
要炼出含铁96%的生铁4000t,至少需要含氧化铁80%的赤铁矿石的质量是多少?(请写出详细的计算过程,结果保留一位小数)
考点:含杂质物质的化学反应的有关计算
专题:有关化学方程式的计算
分析:根据冶炼铁的反应化学方程式,可确定反应中铁与氧化铁的质量关系,利用这一质量关系,可由冶炼铁的质量求得氧化铁的质量,从而计算出所需赤铁矿石的质量.
解答:解:设至少需要含氧化铁80%的赤铁矿石的质量是x.
3CO+Fe2O3
2Fe+3CO2
160 112
80% x 4000t×96%
=
x≈6857.1t
答案:至少需要含氧化铁80%的赤铁矿石6857.1t.
3CO+Fe2O3
| ||
160 112
80% x 4000t×96%
| 160 |
| 112 |
| 80%x |
| 4000t×96% |
x≈6857.1t
答案:至少需要含氧化铁80%的赤铁矿石6857.1t.
点评:根据化学方程式的计算,所使用的物质质量均为纯净物的质量,含杂质的物质质量不能直接代入化学方程式进行计算.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案
相关题目
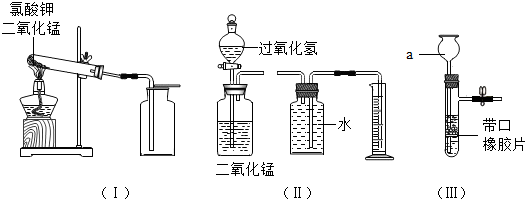
用排水法收集氧气的适宜时间是( )
| A、反应之前就将导管伸入集气瓶 |
| B、气泡均匀连续冒出时收集 |
| C、产生气泡立即收集 |
| D、以上说法都对 |