题目内容
钢铁在生产、生活中有广泛的用途.建造上海世博会的中国馆--“东方之冠”的核心筒就是用四根巨型钢筋混凝土制成的,其中用了大量的钢铁.
(1)钢铁属于 (填“纯净物”或“混合物”);
(2)工业上把铁矿石和焦炭、石灰石一起加入 (写设备名称),在高温下,利用焦炭与氧气反应生成的 把铁从铁矿石里还原出来.请写出一氧化碳与氧化铁在高温下反应的化学方程式: ;
(3)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失.铁在空气中锈蚀,实际上是铁跟空气中的 共同作用的结果;
(4)为了防止钢铁锈蚀,人们常采用 的方法(任写一种)来达到目的.
(5)铝能与NaOH溶液反应:2Al+2NaOH+2H2O=2NaAlO2+3X,X的化学式为 ;
(6)将铝丝浸入硫酸铜溶液中能形成美丽的“铜树”,发生反应的化学方程式为: .
(1)钢铁属于
(2)工业上把铁矿石和焦炭、石灰石一起加入
(3)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失.铁在空气中锈蚀,实际上是铁跟空气中的
(4)为了防止钢铁锈蚀,人们常采用
(5)铝能与NaOH溶液反应:2Al+2NaOH+2H2O=2NaAlO2+3X,X的化学式为
(6)将铝丝浸入硫酸铜溶液中能形成美丽的“铜树”,发生反应的化学方程式为:
考点:生铁和钢,铁的冶炼,金属锈蚀的条件及其防护,纯净物和混合物的判别,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)由多种物质组成的物质属于混合物;
(2)根据炼铁的设备解答;利用焦炭与氧气反应生成的一氧化碳,根据反应物和生成物及其质量守恒定律可以书写化学方程式;
(3)铁与氧气和水充分接触时容易生锈;
(4)使铁与氧气和水隔绝可以防止生锈;
(5)根据化学变化前后原子的种类、数目不变,由反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3X↑,可以推断反应中物质X的分子构成及物质X化学式的确定;
(6)根据反应物和生成物及其质量守恒定律可以书写化学方程式.
(2)根据炼铁的设备解答;利用焦炭与氧气反应生成的一氧化碳,根据反应物和生成物及其质量守恒定律可以书写化学方程式;
(3)铁与氧气和水充分接触时容易生锈;
(4)使铁与氧气和水隔绝可以防止生锈;
(5)根据化学变化前后原子的种类、数目不变,由反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3X↑,可以推断反应中物质X的分子构成及物质X化学式的确定;
(6)根据反应物和生成物及其质量守恒定律可以书写化学方程式.
解答:解:
(1)铁中含碳量较高时,属于生铁,含碳量较低时,属于钢,所以钢铁属于混合物;
(2)工业上把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来,一氧化碳与氧化铁在高温下反应的化学方程式为:3CO+Fe2O3
2Fe+3CO2;
(3)铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果;
(4)在钢铁表面涂漆、镀一层金属等方法可以防止钢铁生锈;
(5)由反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3X↑,
反应前 反应后
Al原子 2 2
Na原子 2 2
O原子 4 4
H原子 6 0
根据化学变化前后原子的种类、数目不变,可判断物质X的每个分子由2个H原子构成,则物质X的化学式为H2;
故答案为:H2;
(6)铝丝浸入硫酸铜溶液中能形成美丽的“铜树”,发生反应的化学方程式为:2A l+3CuSO4═Al2(SO4)3+3Cu
答案:
(1)混合物;
(2)高炉 一氧化碳 3CO+Fe2O3
2Fe+3CO2;
(3)氧气和水
(4)喷漆
(5)H2
(6)2Al+3CuSO4═Al2(SO4)3+3Cu
(1)铁中含碳量较高时,属于生铁,含碳量较低时,属于钢,所以钢铁属于混合物;
(2)工业上把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来,一氧化碳与氧化铁在高温下反应的化学方程式为:3CO+Fe2O3
| ||
(3)铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果;
(4)在钢铁表面涂漆、镀一层金属等方法可以防止钢铁生锈;
(5)由反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3X↑,
反应前 反应后
Al原子 2 2
Na原子 2 2
O原子 4 4
H原子 6 0
根据化学变化前后原子的种类、数目不变,可判断物质X的每个分子由2个H原子构成,则物质X的化学式为H2;
故答案为:H2;
(6)铝丝浸入硫酸铜溶液中能形成美丽的“铜树”,发生反应的化学方程式为:2A l+3CuSO4═Al2(SO4)3+3Cu
答案:
(1)混合物;
(2)高炉 一氧化碳 3CO+Fe2O3
| ||
(3)氧气和水
(4)喷漆
(5)H2
(6)2Al+3CuSO4═Al2(SO4)3+3Cu
点评:解答本题要充分理解质量守恒定律的内容,同时要理解金属生锈的条件,再根据生锈的条件方面进行分析,从而找出保护金属的方法.

练习册系列答案
相关题目
下列几组物质按氧化物、酸、碱、盐顺序排列的是( )
| A、CaO KNO3 NaOH HCl |
| B、CuO Ca(OH)2 HCl NaCl |
| C、H2O H2SO4 Na2CO3 Ba(OH)2 |
| D、CO2 HNO3 KOH CuSO4 |
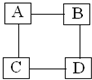 A为金属单质,B、C、D为三种不同类别的化合物,物质间相互反应的关系如图所示(图中“--”表示相连的两种物质能发生反应). 对A、B、C、D各举一具体物质,进行回答:
A为金属单质,B、C、D为三种不同类别的化合物,物质间相互反应的关系如图所示(图中“--”表示相连的两种物质能发生反应). 对A、B、C、D各举一具体物质,进行回答: