题目内容
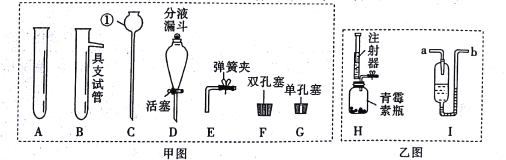
【题目】如图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。试根据题目要求,回答下列问题:
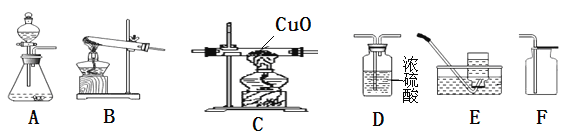
Ⅰ.若用过氧化氢溶液在二氧化锰的催化作用下制取并收集干燥的氧气。
(1)所选仪器的连接顺序为______________(填写仪器序号字母);
(2)制备氧气所发生的化学方程式为____________________________。
Ⅱ.小丽同学欲用下列实验方案测定水中氢、氧元素的质量比,A中盛的是锌粒和稀硫酸,C玻璃管中是氧化铜粉末。气体流向是从左向右,选择的仪器按A→D1→C→D2→D3顺序连接(D1、D2、D3为浓硫酸洗气瓶),然后进行实验(假设有关反应均反应完全)。
(1)仪器D1的作用是______________________________ ;
(2)在发生反应时,装置C应该先_____________(填“加热”或“通入氢气”),观察到装置C中的现象是______________________________;
(3)若测得洗气瓶D2的质量增加mg,而C处大玻璃管内的物质总质量减少ng,则水中氢、氧元素的质量比为_____________(用含m和n的代数式表示);如果不连接仪器D1,则测定结果与实际值比较将_______________(填“偏大”、“偏小”或“基本一致”)。
【答案】 A D F 2H2O2![]() 2H2O +O2↑ 干燥氢气(或吸收氢气中的水分) 通入氢气 黑色粉末变为红色
2H2O +O2↑ 干燥氢气(或吸收氢气中的水分) 通入氢气 黑色粉末变为红色 ![]() 偏大
偏大
【解析】根据所学知识和题中信息知,Ⅰ.用过氧化氢溶液在二氧化锰的催化作用下制取并收集干燥的氧气。(1)所选仪器的连接顺序为A 制取装置,固体和液体不需加热制取气体;D干燥装置,浓硫酸具有吸水性; F收集装置,氧气密度比空气略大。(2)制备氧气所发生的化学方程式为2H2O2![]() 2H2O +O2↑。Ⅱ.用下列实验方案测定水中氢、氧元素的质量比。(1)仪器D1的作用是干燥氢气(或吸收氢气中的水分),浓硫酸具有吸水性;(2)在发生反应时,装置C应该先通入氢气,排净硬质试管中的空气,防止爆炸。观察到装置C中的现象是黑色粉末变为红色,由氧化铜变为铜,氧化铜是黑色,铜是红色。(3)测得洗气瓶D2的质量增加mg,而C处大玻璃管内的物质总质量减少ng,则水中氢、氧元素的质量比为∶
2H2O +O2↑。Ⅱ.用下列实验方案测定水中氢、氧元素的质量比。(1)仪器D1的作用是干燥氢气(或吸收氢气中的水分),浓硫酸具有吸水性;(2)在发生反应时,装置C应该先通入氢气,排净硬质试管中的空气,防止爆炸。观察到装置C中的现象是黑色粉末变为红色,由氧化铜变为铜,氧化铜是黑色,铜是红色。(3)测得洗气瓶D2的质量增加mg,而C处大玻璃管内的物质总质量减少ng,则水中氢、氧元素的质量比为∶
﹙mg-ng﹚∶ng=![]() ;如果不连接仪器D1,则测定结果与实际值比较将偏大,空气中含有水,D2的质量增加大于mg。
;如果不连接仪器D1,则测定结果与实际值比较将偏大,空气中含有水,D2的质量增加大于mg。
点睛∶根据反应物状态和反应条件选择气体制取装置,根据生成物密度和溶解性选择气体收集装置。