题目内容
【题目】实验探究题
同学们为了研究氧化铁能否在氯酸钾制取氧气的实验中起催化作用,进行了以下实验:
[实验一]氧化铁能否在氯酸钾制取氧气的实验中加快反应速率。
实验编号 | KClO3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
1 | 0.6 | - - | 67 | 1800 |
2 | 0.6 | 0.2g二氧化锰 | 67 | 36.5 |
3 | 0.6 | ____________________g氧化铁 | 67 | 89.5 |
(1)实验3中氧化铁的质量为__________________g,以上实验采用了________________的实验方法。
(2)实验一得到的结论是____________。
[实验二]为证明氧化铁是该反应的催化剂,同学们又完成了以下的实验:
[资料]氯酸钾和氯化钾均能溶于水.
I.在实验3反应后的混合物中加足量的水溶解,过滤得到固体,洗涤干燥并用天平称量,质量为0.2g.
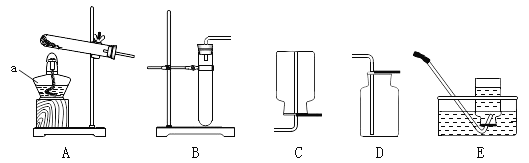
II.将一定量的CO通入滤出的固体,按下面进行实验:
实验装置 | 实验现象 | 实验分析 |
| 玻璃管中固体全部变为黑色 | 生成了铁 |
锥形瓶中澄清石灰水变浑浊 | 产生了二氧化碳 |
(3)写出玻璃管内发生反应的化学方程式____________。写出澄清石灰水变浑浊的化学方程式__________。
[实验结论]氧化铁能在氯酸钾制取氧气反应中起催化作用.
实验反思] (4)小华同学发现实验二( II )中的实验装置从环保角度看有一个缺陷,改进的方法是_____________________________。若该固体完全反应,则实验完冷却试管后,直形试管的质量将_____________(增大\减小),理论上质量的改变量为____________________________克。
(5)同时小华查阅资料发现一氧化碳还原氧化铁后剩余固体可能由氧化亚铁、四氧化三铁、铁粉和未反应的氧化铁中的一种或几种组成.为了研究剩余固体的成分,小红同学查阅了以下资料:
铁粉 | 氧化亚铁 | 氧化铁 | 四氧化三铁 | |
颜色 | 黑色 | 黑色 | 红色 | 黑色 |
磁性 | 有 | 无 | 无 | 有 |
与CO | 不反应 | 反应 | 反应 | 反应 |
与稀盐酸 | 反应生成氯化亚铁和水 | 生成氯化铁和水 | 生成氯化亚铁、氯化铁和水 | |
与硫酸铜溶液 | 反应 | 不反应 | 不反应 | 不反应 |
小红同学认为剩余固体中一定没有氧化铁,原因是_________________。
(6)测定剩余固体的组成.
步骤 | 实验操作 | 实验现象 | 结论和解释 |
用磁铁吸引剩余固体 | ①_________________________, | 剩余固体中没有氧化亚铁 | |
2 | ②______________, | ③_______________, | 剩余固体中只有铁粉 |
【答案】0.2 0.2 对比 氧化铁加快氯酸钾制取氧气的实验中起加快反应速率 Fe2O3+3CO![]() 2Fe+3CO2 CO2+Ca(OH)2=CaCO3↓+H2O 在装置末端玻璃导管处防止一个燃着的酒精的 减小 0.06 氧化铁的颜色为红色,其他物质的颜色都为黑色 剩余固体能够全部被吸引 加入足量的硫酸铜溶液 黑色固体全部溶解,蓝色溶液变为浅绿色有红色固体析出
2Fe+3CO2 CO2+Ca(OH)2=CaCO3↓+H2O 在装置末端玻璃导管处防止一个燃着的酒精的 减小 0.06 氧化铁的颜色为红色,其他物质的颜色都为黑色 剩余固体能够全部被吸引 加入足量的硫酸铜溶液 黑色固体全部溶解,蓝色溶液变为浅绿色有红色固体析出
【解析】
实验一:(1)实验3中氧化铁的质量应该与实验2中二氧化锰的质量相等,0.2g,以上实验采用了对比实验方法;
(2)实验一得到的结论是:氧化铁能在氯酸钾制取氧气的实验中起加快反应速率,因为实验3中,产生相同体积的氧气,加入氯化铁需要的时间比没有加氯化铁需要的时间明显要少;
实验二:(3)玻璃管一氧化碳高温条件下与氧化铁反应产生铁和二氧化碳的化学方程式:Fe2O3+3CO![]() 2Fe+3CO2。
2Fe+3CO2。
二氧化碳与澄清石灰水反应生成碳酸钙沉淀和水的化学方程式:CO2+Ca(OH)2=CaCO3↓+H2O;
(4)小华同学发现实验二( II )中,一氧化碳有毒,不能直接排放到空气中,实验装置从环保角度看有一个缺陷,改进的方法是:在装置末端玻璃导管处防止一个燃着的酒精的;若该固体完全反应,则实验完冷却试管后,氧化铁变为铁,直形试管的质量将减小,理论上质量的改变量为=0.2g×![]() ;
;
(5)小红同学认为剩余固体中一定没有氧化铁,原因是:氧化铁的颜色为红色,其他物质的颜色都为黑色;
步骤 | 实验操作 | 实验现象 | 结论和解释 |
1 | 用磁铁吸引剩余固体 | ①剩余固体能够全部被吸引, | 剩余固体中没有氧化亚铁 |
2 | ②加入足量的硫酸铜溶液, | ③黑色固体全部溶解,蓝色溶液变为浅绿色有红色固体析出, | 剩余固体中只有铁粉 |
1、因为铁粉和四氧化三铁能够被磁铁吸引,而氧化亚铁不能;所以:剩余固体中没有氧化亚铁;
2、因为铁粉能与硫酸铜溶液反应产生红色固体铜和和浅绿色溶液硫酸亚铁溶液,而四氧化三铁不能;所以:剩余固体中只有铁粉;

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案【题目】某兴趣小组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用下图装置完成表中实验:
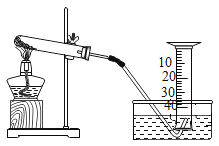
编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50mL O2所需时间/s |
实验1 | 5 | _ | _ | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
(1)设置实验1的目的是_____。
(2)表中所列3种催化剂的催化效果最佳的是_____。
(3)由实验1和实验4可知,KCl_____(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集50mLO2,所需时间明显少于171s,解释原因:_____。