题目内容
【题目】如图是a、b、c三种固体物质的溶解度曲线,下列说法正确的是( )
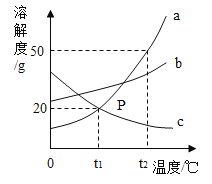
A.a物质的溶解度为50g
B.t2℃时a、b、c的饱和溶液降温到t1℃时,所得溶液溶质质量分数大小关系:b>a>c
C.降低温度一定可使不饱和的a溶液变为饱和
D.将a、b的饱和溶液从t2℃降至t1℃时析出晶体质量a>b
【答案】B
【解析】
A、没有指明温度,不能确定a的溶解度,故错误;
B、将t2℃时a、b、c三种物质的饱和溶液降温到t1℃时,a、b的溶解度减小,c的溶解度随温度的降低而增大,a、b有晶体析出,质量分数变小溶液仍为饱和溶液,c没有晶体析出,质量分数不变,一定温度下饱和溶液的溶质质量分数=![]() ,溶解度越大,质量分数越大,t1℃时b的溶解度大于a的溶解度大于t2℃时c的溶解度,所以t1℃时三种物质的溶质质量分数由大到小的顺序是b>a>c,故正确;
,溶解度越大,质量分数越大,t1℃时b的溶解度大于a的溶解度大于t2℃时c的溶解度,所以t1℃时三种物质的溶质质量分数由大到小的顺序是b>a>c,故正确;
C、如果a的质量很小,溶剂的质量很大,降温时溶液也可能达不到饱和,故错误;
D、由于没有指明溶液的质量关系,无法确定将a、b的饱和溶液从t2℃降至t1℃时析出晶体质量关系,故错误。
故选:B。

 阅读快车系列答案
阅读快车系列答案【题目】工业上制取烧碱的方法之一是电解食盐水法,在生成烧碱的同时还在两电极上产生两种气体(经检验均不是氧气),则该反应的化学方程式为_____。
某化学小组在化工商店购得某品牌的烧碱样品,准备用于化学实验。当将其配制成溶液时,小刚同学观察包装袋标签发现了问题:根据生产日期,这包烧碱存放时间较长,会不会变质呢?于是对这包烧碱进行如下探究:
(一)这包烧碱含有什么成分?
(1)打开后发现样品表面出现一层白色粉末,初步判断已经变质,出现该现象的原因是_____(用化学方程式表示)。
(2)小刚同学猜想:该包烧碱的成分可能是NaOH和Na2CO3也可能完全是Na2CO3。
(3)实验探究:
实验操作 | 现象 | 结论 |
①取少量样品于试管中,完全溶于水,滴加过量的BaCl2溶液 | 产生白色沉淀 | 含有Na2CO3 |
②取①中上层清液,滴加_____试液 | _____ | 还含有NaOH |
反思1:小红同学在实验完成后提出个人质疑:化学反应中的原料往往不能完全转化为产品,所以电解食盐水法制得的烧碱中往往会含有杂质_____(填化学式)。
所以需要进行再探究:另取上述实验①中的上层清液,滴加足量稀硝酸和AgNO3溶液,产生白色沉淀,得出结论,说明小红的质疑是正确的。
反思2:小亮认为,小红的实验设计有缺陷,理由是_____。
(二)成分含量测定

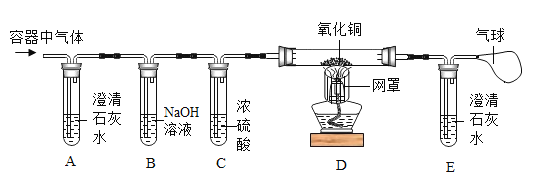
a.取样品mg放入如图装置中加水完全溶解,后放在电子天平上称量为m1g
b.打开分液漏斗活塞加入足量稀硝酸溶液,待反应停止再试样称量为m2g
c.根据化学方程式计算,样品中Na2CO3的质量分数=_____(写出表达式即可,Na2CO3、CO2的相对分子质量分别为106、44)
【题目】用对比实验方法探究二氧化碳的性质。
实验一 |
|
(1)装置l中,将Y形导管平放于桌面上,通入CO2后,观察到a管中试纸_____。通过a、b两管中的实验现象说明CO2的性质是_____(用化学方程式表示)。
(2)装置II中,将Y形管固定在铁架台上,a管在上方,b管在下方,缓缓通入CO2后,通过观察到的现象可说明CO2具有①所验证的性质外,还说明CO2的_____。