题目内容
【题目】(10分)将 146g稀盐酸慢慢加入到24g含有杂质的石灰石(杂质不溶于水也不与酸反应)中,反应情况如图所示。完成以下计算:
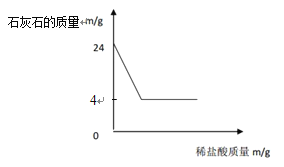
(1)石灰石样品中碳酸钙的质量为多少克?
(2)生成二氧化碳多少克?
(3)求该稀盐酸的溶质质量分数。
【答案】(1)20克(2)8.8克(3)10%
【解析】
试题分析根据图示看,最后剩余的4克属于不能反应的杂质,所以石灰石样品中碳酸钙的质量为=24克-4克=20克。解:设生成二氧化碳的质量为x
CaCO3+2HCl==CaCl2+CO2 ↑ +H2O
100 44
20g x
100/44=20g/x x=8.8g
答:生成二氧化碳的质量为8.8克
解:设该稀盐酸的适量为y
CaCO3+2HCl==CaCl2+CO2 ↑+H2O
100 73
20g y
100/73=20g/y y=14.6g
HCl%=14.6g/146g×100%=10%

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目