题目内容
(6分)氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等。某工厂以石灰石为原料生产二水化钙(CaCl2·2H2O)的流程如下。原料石灰石中含有杂质主要是MgCO3、MgSO4和Al2O3。
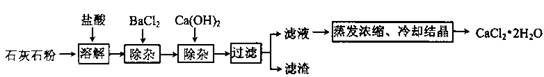
(1)石灰石粉溶解时,Al2O3发生反应的化学方程式为______________。
(2)加入BaCl2除去的杂质离子是__________;加入Ca(OH)2除去的杂质离子是________。
(3)检验“滤液”酸碱性,如果显碱性,还需加入适量的___________________(填化学式)提高产品纯度。

(1)石灰石粉溶解时,Al2O3发生反应的化学方程式为______________。
(2)加入BaCl2除去的杂质离子是__________;加入Ca(OH)2除去的杂质离子是________。
(3)检验“滤液”酸碱性,如果显碱性,还需加入适量的___________________(填化学式)提高产品纯度。
⑴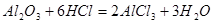
⑵硫酸根离子 镁离子、铝离子(或Mg2+、Al3+)
⑶HCl
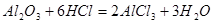
⑵硫酸根离子 镁离子、铝离子(或Mg2+、Al3+)
⑶HCl
分析:(1)氧化铝为金属氧化物,金属氧化物与酸发生复分解反应生成盐和水;
(2)氯化钡能与溶液中的硫酸镁反应生成硫酸钡沉淀,由此可判断加入氯化钡除去了溶液中的硫酸根离子;氢氧化钙能与溶液中氯化镁、氯化铝生成氢氧化镁、氢氧化铝的沉淀,因此,加入的氢氧化钙可除去溶液中镁离子、铝离子;
(3)若滤液呈碱性,可说明前面操作所加氢氧化钙过量,为得到较纯净氯化钙,应加入稀盐酸进行中和.
解:(1)氧化铝与盐酸反应生成氯化铝和水,化学方程式为Al2O3+6HCl=2AlCl3+3H2O;
(2)氯化钡能与溶液中的硫酸镁反应生成硫酸钡沉淀和氯化镁,因此,除去的杂质离子为硫酸根离子;氢氧化钙能与溶液中氯化镁、氯化铝反应生成氢氧化镁沉淀、氢氧化铝沉淀和氯化钙,因此,除去的杂质离子为镁离子、铝离子;
(3)如果滤液显碱性,则前后操作中加入的氢氧化钙过量,可加入稀盐酸与氢氧化钙反应生成氯化钙和水,除去氢氧化钙而得到较为纯净的氯化钙;
故答案为:(1)Al2O3+6HCl=2AlCl3+3H2O;
(2)硫酸根离子;镁离子、铝离子(或Mg2+、Al3+)
(3)HCl.
(2)氯化钡能与溶液中的硫酸镁反应生成硫酸钡沉淀,由此可判断加入氯化钡除去了溶液中的硫酸根离子;氢氧化钙能与溶液中氯化镁、氯化铝生成氢氧化镁、氢氧化铝的沉淀,因此,加入的氢氧化钙可除去溶液中镁离子、铝离子;
(3)若滤液呈碱性,可说明前面操作所加氢氧化钙过量,为得到较纯净氯化钙,应加入稀盐酸进行中和.
解:(1)氧化铝与盐酸反应生成氯化铝和水,化学方程式为Al2O3+6HCl=2AlCl3+3H2O;
(2)氯化钡能与溶液中的硫酸镁反应生成硫酸钡沉淀和氯化镁,因此,除去的杂质离子为硫酸根离子;氢氧化钙能与溶液中氯化镁、氯化铝反应生成氢氧化镁沉淀、氢氧化铝沉淀和氯化钙,因此,除去的杂质离子为镁离子、铝离子;
(3)如果滤液显碱性,则前后操作中加入的氢氧化钙过量,可加入稀盐酸与氢氧化钙反应生成氯化钙和水,除去氢氧化钙而得到较为纯净的氯化钙;
故答案为:(1)Al2O3+6HCl=2AlCl3+3H2O;
(2)硫酸根离子;镁离子、铝离子(或Mg2+、Al3+)
(3)HCl.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目