��Ŀ����
����Ŀ��ij�о���ѧϰС������������װ�ý������������ȡ��̽���������������գ� 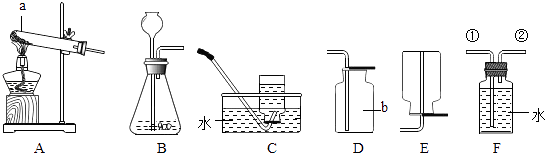
��1��д��ͼ������a��b������ a �� b ��
��2��ʵ������ȡ������̼�Ļ�ѧ����ʽ�� �� Ӧѡ������巢��װ���� �� �����ռ�װ���� ��
��3��ʵ���Ҽ�������غͶ���������ȡ�����Ļ�ѧ����ʽ�� �� Ӧѡ��ķ���װ���� �� ����ʢ��ˮ��Fװ���ռ�������Ӧ�ӵ�������ٻ�ڣ�ͨ�룮
��4��������һ����ɫ����ζ��������ˮ���ܶ�С�ڿ����ܶȵ����壬ʵ�����ü�����ˮ�����ƺͼ�ʯ�ҵĹ�������ķ�����ȡ���飬��ʵ������ȡ���ռ�����Ӧѡ���װ������� ��
���𰸡�
��1���Թܣ�����ƿ
��2��CaCO3+2HCl�TCaCl2+H2O+CO2����B��D
��3��2KClO3 ![]() 2KCl+3O2����A����
2KCl+3O2����A����
��4��AC��AE
���������⣺��1��ͼ��a����������Һ��ij���©����b�������ռ�����ļ���ƿ�����Դ��ǣ�����©��������ƿ����2��ʵ������ȡ������̼�Ļ�ѧ��Ӧʽ�ǣ�CaCO3+2HCl�TCaCl2+H2O+CO2�����˷�Ӧ�ǹ�Һ�����ȷ�Ӧ������װ��B��Ϊ����װ�ã��������̼���ܶȴ��ڿ������ܶȣ�����������ˮ���ʿ���D�����ſ������ռ����壮���Դ��ǣ�CaCO3+2HCl�TCaCl2+H2O+CO2����B��D����3��ʵ���Ҽ�������غͶ���������ȡ�����Ļ�ѧ����ʽ�ǣ�2KClO3 ![]() 2KCl+3O2�������ǹ���ļ��ȷ�Ӧ�����Կ���װ��A��Ϊ����װ�ã���ʢ��ˮ��Fװ���ռ��������൱����ˮ���ռ�����������ɴӢڽ��룬ˮ���Ӣ��ų������Դ��ǣ�2KClO3
2KCl+3O2�������ǹ���ļ��ȷ�Ӧ�����Կ���װ��A��Ϊ����װ�ã���ʢ��ˮ��Fװ���ռ��������൱����ˮ���ռ�����������ɴӢڽ��룬ˮ���Ӣ��ų������Դ��ǣ�2KClO3 ![]() 2KCl+3O2����A���ڣ���4������ȡ�����Ǽ�����ˮ�����ƺͼ�ʯ�ҵĹ�������ǹ̹̼��ȷ�Ӧ����ѡ�õķ���װ����A���������ܶ�С�ڿ������ܶȣ�����������ˮ������C��ˮ���ռ�����E�����ſ������ռ��� ���Դ��ǣ�AC��AE��
2KCl+3O2����A���ڣ���4������ȡ�����Ǽ�����ˮ�����ƺͼ�ʯ�ҵĹ�������ǹ̹̼��ȷ�Ӧ����ѡ�õķ���װ����A���������ܶ�С�ڿ������ܶȣ�����������ˮ������C��ˮ���ռ�����E�����ſ������ռ��� ���Դ��ǣ�AC��AE��
�����㾫�������ڱ��⿼�����������ȡװ�ú��������ռ���������Ҫ�˽ⷢ��װ�ã��̹̼����͡���Һ�������ͣ��ռ�װ�ã��������ʵ��ܶȡ��ܽ��ԣ���ˮ���ռ�ʱ�������ݾ�������ð��ʱ���ռ����տ�ʼ�ų������Թ��еĿ����������ſ������ռ�����ʱ�������쵽����ƿ�ײ����ܵó���ȷ�𰸣�

����Ŀ��Fe2O3��һ�������¿�ת��ΪFeO��Fe2O3+CO ![]() 2FeO +CO2 �� ��ӦǰFe2O3������Ϊ160�ˣ���Ӧ�����У�Fe2O3��ת���ʣ��μӷ�Ӧ��Fe2O3�뷴Ӧǰ��Fe2O3�������ȣ���a��ʾ����������Ԫ������Ԫ�ص���������mFe/m Fe0��ʾ��
2FeO +CO2 �� ��ӦǰFe2O3������Ϊ160�ˣ���Ӧ�����У�Fe2O3��ת���ʣ��μӷ�Ӧ��Fe2O3�뷴Ӧǰ��Fe2O3�������ȣ���a��ʾ����������Ԫ������Ԫ�ص���������mFe/m Fe0��ʾ��
��1����д�±��еĿո�
mFe/m 0 | 7/3 | 14/5 | 7/2 |
����ɷ� | Fe2O3 | Fe2O3��FeO | |
ת���ʣ����� | 0 | 100% |
��2�����Fe2O3ת��ΪFeO �ķ�Ӧ���������У�3Fe2O3+CO ![]() 2Fe3O4+CO2 Fe304+3CO
2Fe3O4+CO2 Fe304+3CO ![]() 2FeO+CO2��Ӧ��Ĺ�����mFe/mO�T21/8ʱ����ijɷֿ��������������
2FeO+CO2��Ӧ��Ĺ�����mFe/mO�T21/8ʱ����ijɷֿ��������������
��Fe3O4��
�����ѧʽ����ͬ����
��3�� ��