题目内容
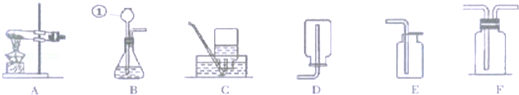
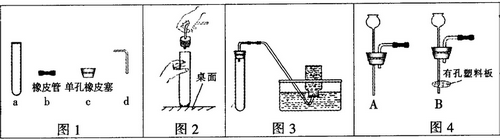
请根据下列实验装置回答问题。

⑴ 写出标有序号的仪器名称:a ,b 。
⑵ 在实验室中用过氧化氢溶液和二氧化锰混合制取氧气时,其中二氧化锰起 作用,发生反应的化学方程式为 。
⑶ 实验室制取二氧化碳气体,应选用的发生装置是 (填写装置的字母代号,下同);检验二氧化碳应选用的装置是 。
 ⑷ 实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3)。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,对人体特别是粘膜组织有腐蚀作用。
⑷ 实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3)。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,对人体特别是粘膜组织有腐蚀作用。
① 制取氨气反应的化学方程式:2NH4Cl + Ca(OH)2 CaCl2 + 2NH3↑+ 2X 。
X的化学式为: 。
② 制取并收集NH3,从上图中选择 和 。
用右图装置收集氨气时,观察到 现象说明氨气已收满。
③ 干燥时不能选用下列干燥剂中的 (填序号)。
A.固体氢氧化钠 B.浓硫酸 C.生石灰

⑴ 写出标有序号的仪器名称:a ,b 。
⑵ 在实验室中用过氧化氢溶液和二氧化锰混合制取氧气时,其中二氧化锰起 作用,发生反应的化学方程式为 。
⑶ 实验室制取二氧化碳气体,应选用的发生装置是 (填写装置的字母代号,下同);检验二氧化碳应选用的装置是 。
 ⑷ 实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3)。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,对人体特别是粘膜组织有腐蚀作用。
⑷ 实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3)。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,对人体特别是粘膜组织有腐蚀作用。① 制取氨气反应的化学方程式:2NH4Cl + Ca(OH)2 CaCl2 + 2NH3↑+ 2X 。
X的化学式为: 。
② 制取并收集NH3,从上图中选择 和 。
用右图装置收集氨气时,观察到 现象说明氨气已收满。

③ 干燥时不能选用下列干燥剂中的 (填序号)。
A.固体氢氧化钠 B.浓硫酸 C.生石灰
⑴①酒精灯 ②铁架台
⑵ 催化 2H2O2MnO2 2H2O+O2↑
⑶ B F ⑷①H2O ②A D 酚酞变红 ③B
⑵ 催化 2H2O2MnO2 2H2O+O2↑
⑶ B F ⑷①H2O ②A D 酚酞变红 ③B
试题分析:(1)根据实验室常用仪器的名称回答,图中仪器a的名称是酒精灯,b是铁架台。
(2)实验室常用过氧化氢在二氧化锰的催化作用下,分解制取氧气,同时还生成水,故反应的化学方程式为2H2O2
 2H2O+O2↑。
2H2O+O2↑。(3)实验室常用石灰石或大理石(固体)和稀盐酸(液体)在常温下反应,来制取二氧化碳气体,故该反应属于“固液体在不加热的条件下的反应”,故发生装置应选固液不加热型装置,故选B;检验二氧化碳气体,要用澄清石灰水,故应选用的装置是F。
(4)①由反应的化学方程式2NH4Cl + Ca(OH)2 CaCl2 + 2NH3↑+ 2X可知,
反应前 反应后
N原子 2 2
H原子 10 6
Cl原子 2 2
Ca原子 1 1
O原子 2 0
根据质量守恒定律,化学变化前后原子的种类、数目不变,可判断生成物2X分子中含有4个H原子和2个O原子,故1个X分子中含有2个H原子和1个O原子,则物质X的化学式为H2O。
② 根据题意,“实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3)”,故属于“固体加热型”,故发生装置应选A;由于氨气的密度小于空气,且极易溶于水,故可用向下排空气法D收集氨气。
如用右图装置收集氨气,当氨气集满时,多余的氨气就会进入右边滴有酚酞的蒸馏水中,氨水呈碱性,故能使其显红色。
③由于氨气能与硫酸溶液反应,故不能用浓硫酸干燥氨气。故选B
点评:熟记氧气和二氧化碳的实验室制法、原理和操作注意事项,是解题的关键;此外,本题的重点是常用气体的发生装置和收集装置的选取方法,要学会根据反应物的状态和反应的条件选择发生装置,根据制取气体的溶解性和密度的大小选择收集气体的方法。

练习册系列答案
相关题目





 (选填>、<或=),则假设二成立;若m
(选填>、<或=),则假设二成立;若m