题目内容
【题目】某班同学用氢氧化钠溶液和稀盐酸进行中和反应实验。
(1)甲同学实验操作如图。
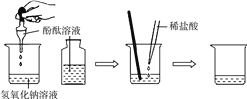
在烧杯中加入约5 mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈________色。
使用胶头滴管吸取液体时,要先按着_______排干净_______,再放入滴瓶中吸取液体。
接着用滴管滴入一定量的稀盐酸,再用玻璃棒搅拌,发现溶液为无色,于是甲同学得出两者恰好中和的结论,反应的化学方程式为________________________________________。
(2)乙同学对甲同学的结论提出了质疑,并对反应后溶液中的溶质成分进行探究。
【实验探究】
反应后溶液中的溶质是什么?
猜想一:只有NaCl。 猜想二:NaCl和HCl。猜想三:NaCl和NaOH。
以上猜想中,你觉得不合理的是______________________。
为了验证另外两种猜想,乙同学设计如下实验方案:
实验操作 | 实验现象 | 实验结论 |
取少量反应后的溶液于试管中滴入Na2CO3溶液 | _______________ | 猜想二成立 |
取少量反应后的溶液于试管中加入锌粒 | _______________ | 猜想一成立 |
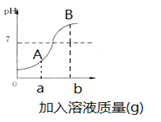
(3)如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是(_______)(多选)
A.该反应是稀HCl滴入NaOH溶液中
B.ag是指加入氢氧化钠固体质量
C.A点溶液的溶质为HCl和NaCl
D.检验B点溶液的溶质先滴加足量的Mg(NO3)2,静置后再滴入少量AgNO3
【答案】 红 橡胶帽 空气 NaOH +HCl==NaCl+H2O 猜想二 产生气泡 无气泡产生(无明显现象) CD
【解析】在烧杯中加入约5 mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈红色。使用胶头滴管吸取液体时,要先按着橡胶帽排干净空气,再放入滴瓶中吸取液体。接着用滴管滴入一定量的稀盐酸,再用玻璃棒搅拌,发现溶液为无色,于是甲同学得出两者恰好中和的结论,反应的化学方程式为NaOH +HCl=NaCl+H2O 。(2) 【实验探究】反应后溶液中的溶质是什么?猜想一:只有NaCl。 猜想二:NaCl和HCl。猜想三:NaCl和NaOH。不合理的是猜想二。验证另外两种猜想,乙同学设计如下实验方案:
实验操作 | 实验现象 | 实验结论 |
取少量反应后的溶液于试管中滴入Na2CO3溶液 | 产生气泡 | 猜想二成立 |
取少量反应后的溶液于试管中加入锌粒 | 无气泡产生 | 猜想一成立 |
(3)如图是稀HCl和NaOH溶液反应的pH变化曲线∶A.该反应是NaOH溶液滴入稀HCl中,起初PH<7,溶液呈酸性。故A错误。B.ag是指加入氢氧化钠溶液的质量。故B错误。C.A点盐酸过量,溶液的溶质为HCl和NaCl。故C正确。D.检验B点氢氧化钠溶液过量,溶质是氢氧化钠和氯化钠,溶液的溶质先滴加足量的Mg(NO3)2,静置后再滴入少量AgNO3。 故D正确。
点睛∶本题主要考查氢氧化钠溶液和稀盐酸进行中和反应实验。

 阅读快车系列答案
阅读快车系列答案【题目】分类是学习和研究化学常用的方法。下列关于物质分类中正确的是( )
A. 混合物:煤、石油、冰水混合物 B. 有机物:甲烷、乙醇、葡萄糖
C. 酸:硫酸、盐酸、碳酸钠 D. 单质:干冰、金刚石、氧气
【题目】除去溶液中的少量杂质,试剂选择正确的是:( )
选项 | 溶液 | 杂质 | 试剂 |
A. | NaNO3 | Na2CO3 | 适量BaCl2溶液 |
B. | CaCl2 | 稀盐酸 | 足量CaCO3固体 |
C. | ZnSO4 | CuSO4 | 足量铜粉 |
D. | Fe2(SO4)3 | Na2SO4 | 适量NaOH溶液 |
A. A B. B C. C D. D

