题目内容
随着人民生活水平的不断提高,各种电池的用量大幅增加,废电池回收集中处理的问题被提到议事日程上来。回收废电池主要是为了
[ ]
A. 利用废电池外壳的金属材料
B. 利用废电池外壳的石墨电极
C. 防止废电池中铅. 镉. 汞等重金属对土壤和水源的污染
D. 防止废电池中渗透的液体对其他物品的腐蚀
B. 利用废电池外壳的石墨电极
C. 防止废电池中铅. 镉. 汞等重金属对土壤和水源的污染
D. 防止废电池中渗透的液体对其他物品的腐蚀
C

练习册系列答案
相关题目
随着人民生活水平的提高,食品安全问题倍受社会关注.苯甲酸是常见的食品防腐剂.它是一种片状晶体,在水中的溶解度如下表:
| 温度 | 25℃ | 50℃ | 95℃ |
| 溶解度 | 0.17g | 0.95g | 6.8g |
(1)提纯苯甲酸:室温下,取样品约10g放入大烧杯中,加入500mL蒸馏水充分搅拌,发现样品几乎没溶解,原因是________,将烧杯放在石棉网上加热,将样品充分溶解后,在加入少量蒸馏水,然后趁热过滤.趁热过滤的目的是________,将所得滤液________,使苯甲酸以晶体形式析出,然后过滤得到较纯净的苯甲酸晶体6.1g.
(2)化学组成分析(苯甲酸中一定含有C、H元素,可能含有氧元素)
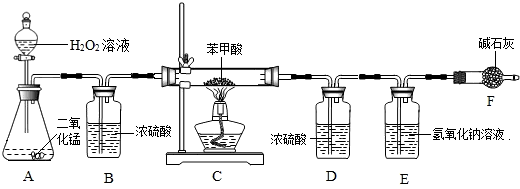
①仪器A中所发生的反应化学方程式为________.
②仪器B的作用是________.
③实验结束后发现装置D增重2.7g,装置E增重15.4g,试通过计算确定苯甲酸中________氧元素(填“含有”或“不含有”),苯甲酸的化学式为________.
随着人民生活水平的提高,食品安全问题倍受社会关注。苯甲酸是常见的食品防腐剂。它是一种片状晶体,在水中的溶解度如下表:
| 温度 | 25℃ | 50℃ | 95℃ |
| 溶解度 | 0.17g | 0.95g | 6.8g |
某研究性学习小组要确定苯甲酸的组成,现有苯甲酸样品(含泥沙等难溶于水的杂质),实验步骤如下:
(1)提纯苯甲酸:室温下,取样品约10g放入大烧杯中,加入500mL蒸馏水充分搅拌,发现样品几乎没溶解,原因是 ,将烧杯放在石棉网上加热,将样品充分溶解后,在加入少量蒸馏水,然后趁热过滤.趁热过滤的目的是 ,将所得滤液 ,使苯甲酸以晶体形式析出,然后过滤得到较纯净的苯甲酸晶体6.1g。
(2)化学组成分析(苯甲酸中一定含有C、H元素,可能含有氧元素)

A B C D E
①仪器A中所发生的反应化学方程式为 。
②仪器B的作用是 。
③实验结束后发现装置D增重2.7g,装置E增重15.4g,试通过计算确定苯甲酸中_______氧元素(填“含有”或“不含有”),苯甲酸的化学式为________________。
