题目内容
【题目】下列所示的图象能正确的反映相对的实验的是( )
A.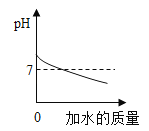 向pH=12的Ca(OH)2溶液中不断加水稀释
向pH=12的Ca(OH)2溶液中不断加水稀释
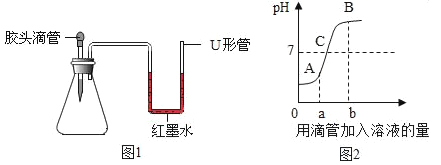
B.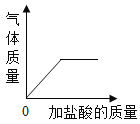 向NaOH和Na2CO3的混合溶液中逐滴加入稀盐酸至过量
向NaOH和Na2CO3的混合溶液中逐滴加入稀盐酸至过量
C.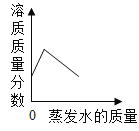 在40°C,将饱和的硝酸钾溶液恒温蒸发至有白色晶体析出
在40°C,将饱和的硝酸钾溶液恒温蒸发至有白色晶体析出
D.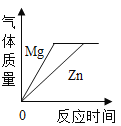 将足量的金属镁、锌分别和等质量的10%的稀硫酸混合
将足量的金属镁、锌分别和等质量的10%的稀硫酸混合
【答案】D
【解析】
解:A、碱性溶液在稀释的过程中,pH会逐渐减小,但是溶液的pH值只会无限的接近7,永远不会越过7,故A错误;
B、向NaOH和Na2CO3的混合溶液中逐滴加入稀盐酸至过量,盐酸会先与氢氧化钠反应,然后再与碳酸钠反应,所以加入一定量的盐酸后才会生成二氧化碳,故B错误;
C、恒温蒸发饱和硝酸钾溶液时,溶液一直是该温度下的饱和溶液,所以溶质的质量分数应不变,故C错误;
D、足量镁和锌分别与等质量的10%的稀硫酸反应时,生成的氢气质量相等,镁比锌活泼,所以镁的反应速率比锌的大,在坐标中镁对应的速率斜线比锌陡,故D正确.
故选:D.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】某密闭容器中有X、氧气和二氧化碳三种物质,在一定条件下充分反应,测得反应前后各物质的质量如表。根据表中信息,判断下列说法不正确的是( )
物质 | X | 氧气 | 二氧化碳 | 水 |
反应前/g | 8 | 36 | 2 | 0 |
反应后/g | 0 | 待测 | 24 | 18 |
A.该反应不是置换反应B.生成二氧化碳与水的质量比为11:9
C.X中碳、氢原子个数比为1:4D.X含有碳氢氧三种元素