题目内容
【题目】具有可变价的金属往往只有一种价态较稳定:铁以+3价、铜以+2价较稳定,而汞以0价较稳定。下列金属硫化物在空气中灼烧时均产生SO2气体。试写出它们在空气中灼烧的化学方程式。
(1)FeS:_________________________________________。
(2)HgS:_________________________________________。
【答案】4FeS+7O2![]() 2Fe2O3+4SO2 HgS+O2
2Fe2O3+4SO2 HgS+O2![]() Hg+SO2
Hg+SO2
【解析】
(1)铁以+3价较稳定,所以FeS在空气中灼烧时除了产生SO2气体,还生成Fe2O3,故灼烧的化学方程式:4FeS+7O2![]() 2Fe2O3+4SO2
2Fe2O3+4SO2
(2)汞的0价较稳定,所以HgS在空气中灼烧时除了产生SO2气体,还生成单质Hg,故灼烧的化学方程式:HgS+O2![]() Hg+SO2
Hg+SO2

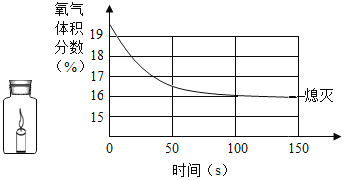
【题目】某研究性学习小组用如图所示装置进行如下实验(不考虑气体与水或盐的反应)
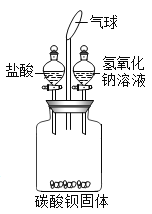
(1)先向广口瓶中加入一定量盐酸溶液至固体恰好全部溶解为止,关闭活塞,振荡,观察到气球变大。然后再将一定量氢氧化钠溶液加入广口瓶中,关闭活塞,振荡,发现气球明显变小,请写出引起气球变小的化学反应方程式_______________,同时在广口瓶中还能观察到的现象是____________。
(2)实验结束后,同学们对广口瓶中的溶液进行探究。
(提出问题)广口瓶中的溶液含有哪些溶质?
(交流讨论)经过大家对广口瓶中所发生的反应进行分析,认为瓶内一定含有的一种溶质是(填化学式,下同)___________。小明取广口瓶内溶液少量于试管中,向其中加入过量稀盐酸,发现有气泡产生.由此得出结论:广口瓶溶液中还含有的溶质是__________。小红认为,可能还存在BaCl2,大家一致认为小红的结论是错误的,理由是__________________。后经大家讨论,达成共识:广口瓶溶液中还可能存在NaOH。
(实验设计)
考虑到已经确定的两种溶质中有一种溶质的存在对氢氧化钠的检验造成干扰,设计方案先将它除去后再检验。具体步骤如下:
实验目的 | 实验步骤 | 实验现象 | 实验结论 |
除去干扰物 | ① 取广口瓶中溶液少量于试管中,向其中加入过量________溶液,充分反应后过滤 | 有白色沉淀产生 | 溶质中还含有NaOH |
检验是否含有NaOH | 在滤液中滴加酚酞试液 | ________ |