��Ŀ����
����Ŀ����7�֣������ҿ�CaO��MgO������������K2SO4�ʼ����ظ��Ϸʡ�
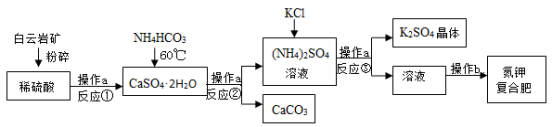
��1���������ҿ�ʯ�����Ŀ�� ��
��2������a�� ���õ��IJ������������������� ������������ ��
��3����Ӧ�ڻ�ѧ����ʽΪCaSO4��2H2O+2NH4HCO3=CaCO3��+(NH4)2SO4+CO2��+3H2O���÷�Ӧ�¶��������60�����ң�ԭ�� ��
��4��K2SO4��ˮ���ܽ��С�ڣ�NH4��2SO4��д����Ӧ�۵Ļ�ѧ����ʽ ������b�IJ��裺 ����ȴ�ᾧ�����˶��õ����ظ��Ϸʡ�
���𰸡���1������Ӵ������ʹ��Ӧ��ֽ��У�
��2������ �� �ձ���©���� ������
��3���ӿ�÷�Ӧ�����ҷ�ֹ̼��������ȷֽ�
��4��(NH4)2SO4+2KCl===K2SO4��+2NH4Cl�� ����Ũ��
��������
����������������ҿ�ʯ�����Ŀ������Ӵ������ʹ��Ӧ��ֽ��У�����a�ܵõ����壬�����ǹ��ˣ��õ��IJ��������������������ձ���©��������������������Ӧ�¶��������60�����ң�ԭ���ӿ�÷�Ӧ�����ҷ�ֹ̼��������ȷֽ⣻����b�ܵõ��������Բ����IJ�������Ũ����

��ϰ��ϵ�д�
 ����С��ʿ���������ϵ�д�
����С��ʿ���������ϵ�д�
�����Ŀ