题目内容
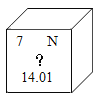
【题目】下列叙述对应的化学方程式、所属基本反应类型都正确的是( )
A.服用含氢氧化铝的药物治疗胃酸过多 Al(OH)3+3HCl=AlCl3+3H2O 复分解反应
B.不能用铁桶盛放波尔多液 Fe+CuSO4=Cu+FeSO4 分解反应
C.用天然气作燃料 CH4+O2![]() CO2+2H2O 氧化反应
CO2+2H2O 氧化反应
D.验证铜和铝的活动性 3Cu+A12(SO4)3=3CuSO4+2Al 置换反应
【答案】A
【解析】
根据反应原理找出反应物、生成物、反应条件,并根据化学方程式进行判断。
A、胃酸中主要成分是HCl,属于酸,药物中的氢氧化铝成分是Al(OH)3,属于碱。胃酸中的盐酸会和药物中的碱氢氧化铝发生复分解反应,生成一种盐氯化铝和水。故A正确;
B、农药波尔多液的主要成分是硫酸铜。若用铁桶盛放,铁会和硫酸铜反应生成硫酸亚铁和铜。反应是由一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应。故B错误;
C、天然气的主要成分是甲烷(CH4)。甲烷充分燃烧时,在点燃的条件下,甲烷会和空气中的氧气发生化学反应,生成二氧化碳和水。该反应不属于四大基本反应类型中的任何一种,且方程式未配平。故C错误;
D、验证铝和铜的活动性,铝的金属活动性比铜强,故铝能将铜从它的盐溶液中置换出来,而铜无法置换出盐溶液中的铝。故D错误。
故选A。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案【题目】铁、铝、铜是常见的三种金属。同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理。
(提出问题)这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
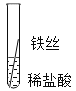
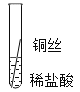
(实验探究)同学们对三种金属的活动性顺序展开了探究,请你参与探究并填写空格。将粗细相同的铁丝、铝丝、铜丝分别插入体积相同溶质质量分数也相同的稀盐酸中:
操作 |
|
|
| 根据现象得出金属活动性顺序 |
片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 |
|
几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 | _________________ |
(讨论交流)为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面致密的氧化膜会先与稀盐酸反应。
(反思评价)做金属性质实验时需将金属进行打磨,打磨的目的是_________________。
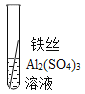
(实验验证)为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
操作 |
|
| 根据现象得出三种金属活动性顺序 |
现象 | 无明显现象 | ___________________ |
|
写出铁与硫酸铜溶液反应的化学方程式___________________________。
(拓展迁移)
(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插入顺序(能与稀盐酸反应的要一次将稀盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序。金属丝的插入顺序为_________。
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序___________________________。