题目内容
 从HCl,NaOH,NaCl,Na2CO3,Ca(OH)2几种溶液中取出其中的两种混合:
从HCl,NaOH,NaCl,Na2CO3,Ca(OH)2几种溶液中取出其中的两种混合:(1)若混合后溶液质量减小的组合是
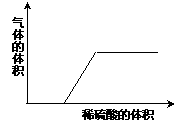
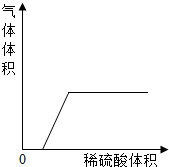
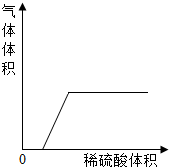
(2)若混合溶液质量不变,但滴入稀硫酸后产生气体的质量与加入稀H2SO4的关系如图所示,则组合为
分析:(1)两种溶液混合后质量减小,可能的原因是两种溶液混合后发生化学反应,生成气体或沉淀,从溶液中分离开来;
(2)弄清图象表示的意义:刚开始时没有气泡生成,说明混合溶液中一定含有碱,而过一段时间后有气泡产生说明混合物中一定含有碳酸钠.
(2)弄清图象表示的意义:刚开始时没有气泡生成,说明混合溶液中一定含有碱,而过一段时间后有气泡产生说明混合物中一定含有碳酸钠.
解答:解:(1)本题中的HCl和Na2CO3混合后,会发生化学反应(Na2CO3+2HCl=2NaCl+H2O+CO2↑)产生的二氧化碳扩散导致反应后所得溶液质量变小;Na2CO3和Ca(OH)2混合后,会发生化学反应(Ca(OH)2+Na2CO3═CaCO3↓+2NaOH)产生的碳酸钙难溶于水而从溶液中分离出来,导致反应后所得溶液质量变小.
故答案为:HCl和Na2CO3;Na2CO3和Ca(OH)2.
(2)根据图象可以看出有气泡冒出,则混合溶液中一定有碳酸钠,而刚开始时无气泡产生,说明混合溶液中有能够和酸先反应但不能和碳酸钠反应的物质,因此另外一种物质可以是氢氧化钠,故答案为:NaOH、Na2CO3.
故答案为:HCl和Na2CO3;Na2CO3和Ca(OH)2.
(2)根据图象可以看出有气泡冒出,则混合溶液中一定有碳酸钠,而刚开始时无气泡产生,说明混合溶液中有能够和酸先反应但不能和碳酸钠反应的物质,因此另外一种物质可以是氢氧化钠,故答案为:NaOH、Na2CO3.
点评:本题以溶液质量的变化为背景考查复分解反应发生的条件及根据反应的现象分析具体的反应情况,培养学生分析问题的能力.熟悉酸、碱、盐的化学性质是解答此类题的关键.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
 从HCl,NaOH,NaCl,Na2CO3,Ca(OH)2几种溶液中取出其中的两种混合:
从HCl,NaOH,NaCl,Na2CO3,Ca(OH)2几种溶液中取出其中的两种混合: