题目内容
从HCl、NaOH、Na2CO3、Ca(OH)2几种溶液中取出其中的两种混合.
(1)若混合后溶液质量减小,可能的组合是:________、________.
(2)若混合后溶液质量不变,但发生了化学反应,有关的化学方程式为:________、________.
(3)实验后若将所有的废液倒入同一洁净的烧杯中.除指示剂外,最终烧杯中一定含有的溶质是________.
解:(1)碳酸钠与盐酸反应后生成二氧化碳气体,导致溶液质量减小,碳酸钠与氢氧化钙溶液反应后生成碳酸钙沉淀,导致溶液质量减小,故填:HCl和Na2CO3,Na2CO3和Ca(OH)2;
(2)混合后溶液质量不变,则反应时没有沉淀或气体生成,生成的是水,则是酸和碱的反应,可以是氢氧化钠和盐酸反应生成氯化钠和水,可以是氢氧化钙和盐酸反应生成氯化钙和水,故填:NaOH+HCl=NaCl+H2O,Ca(OH)2+2HCl=CaCl2+2H2O;
(3)根据物质所含有的离子,最终反应后,氢离子能与氢氧根离子结合生成水分子,碳酸根离子能与钙离子结合生成碳酸钙沉淀,最终剩余的滤液中一定含有NaCl,故填:NaCl.
分析:根据已有的知识进行分析,混合后溶液质量减小,则反应生成了气体或沉淀,混合后溶液质量不变,则反应没有沉淀或气体生成,根据物质之间的反应进行解答即可.
点评:本题考查了复分解反应的条件,完成此题,可以依据具体物质的性质结合复分解反应的条件进行.
(2)混合后溶液质量不变,则反应时没有沉淀或气体生成,生成的是水,则是酸和碱的反应,可以是氢氧化钠和盐酸反应生成氯化钠和水,可以是氢氧化钙和盐酸反应生成氯化钙和水,故填:NaOH+HCl=NaCl+H2O,Ca(OH)2+2HCl=CaCl2+2H2O;
(3)根据物质所含有的离子,最终反应后,氢离子能与氢氧根离子结合生成水分子,碳酸根离子能与钙离子结合生成碳酸钙沉淀,最终剩余的滤液中一定含有NaCl,故填:NaCl.
分析:根据已有的知识进行分析,混合后溶液质量减小,则反应生成了气体或沉淀,混合后溶液质量不变,则反应没有沉淀或气体生成,根据物质之间的反应进行解答即可.
点评:本题考查了复分解反应的条件,完成此题,可以依据具体物质的性质结合复分解反应的条件进行.

练习册系列答案
相关题目
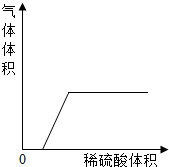 从HCl,NaOH,NaCl,Na2CO3,Ca(OH)2几种溶液中取出其中的两种混合:
从HCl,NaOH,NaCl,Na2CO3,Ca(OH)2几种溶液中取出其中的两种混合: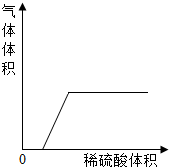 从HCl,NaOH,NaCl,Na2CO3,Ca(OH)2几种溶液中取出其中的两种混合:
从HCl,NaOH,NaCl,Na2CO3,Ca(OH)2几种溶液中取出其中的两种混合: