题目内容
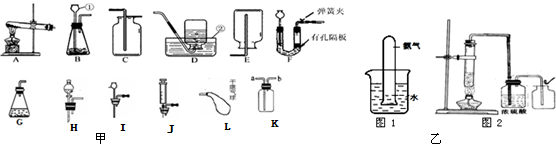
根据下列装置图1,回答有关问题: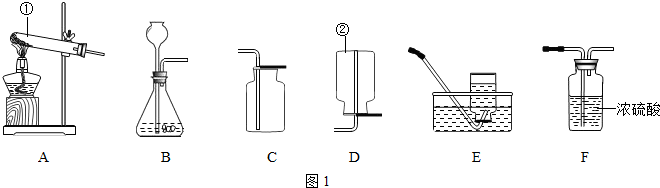
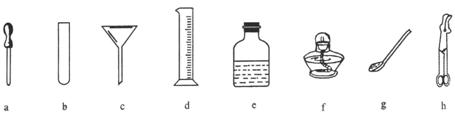
(1)写出装置图中标号仪器的名称:①
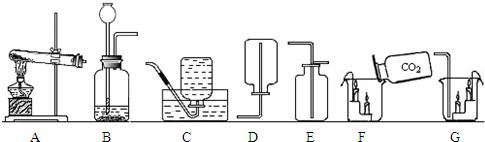
(2)实验室制取二氧化碳的反应化学方程式为
(3)如选用装置A作为制取氧气的发生装置,其化学方程式可以为
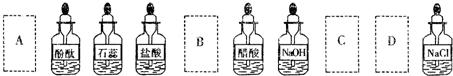
(4)要鉴别氧气和二氧化碳,不可行的是
A.无色酚酞溶液 B.紫色石蕊溶液
C.澄清石灰水 D.燃着的木条.
分析:(1)根据仪器的形状、结构、用途回答.
(2)根据实验室制二氧化碳的原理,气体发生装置和收集装置的选择依据回答.
(3)根据实验室制氧气的原理及气体发生装置和收集装置的选择依据回答.
(4)根据二氧化碳和氧气的性质判断.
(2)根据实验室制二氧化碳的原理,气体发生装置和收集装置的选择依据回答.
(3)根据实验室制氧气的原理及气体发生装置和收集装置的选择依据回答.
(4)根据二氧化碳和氧气的性质判断.
解答:解:
(1)①为少量试剂的反应容器,也能给少量液体加热,为试管;②是收集气体的仪器,为集气瓶.
(2)实验室制二氧化碳的原理是碳酸钙与盐酸反应生成氯化钙、水、二氧化碳,方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;用的药品是固体石灰石和液体稀盐酸,反应不需要加热,发生装置用B,二氧化碳溶解于水,密度比空气大,收集装置选C;浓硫酸有吸水性,干燥二氧化碳用浓硫酸,故还需F装置.
(3)装置A是加热固体制氧气的装置,且试管口没有一团棉花,适于加热氯酸钾和二氧化锰混合物制氧气,方程式为:2KClO3
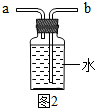
2KCl+3O2↑;图2所示装置收集氧气实际上是排水法,水只能从长管排出,氧气应从a 端导入.(4)A、氧气和二氧化碳都不能使无色酚酞溶液变色,不可行,所以正确.
B、氧气不能使紫色石蕊溶液变色,二氧化碳能使紫色石蕊溶液变红色,
C、氧气不能使澄清石灰水变浑,二氧化碳能使澄清石灰水变浑,是可行的,所以错误.
D、氧气能使燃着的木条燃烧更旺,二氧化碳能使燃着的木条熄灭,是可行的,所以错误.
故答案为:(1)①试管;②集气瓶;(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;BFC;(3)2KClO3
2KCl+3O2↑;a;(4)A.
(1)①为少量试剂的反应容器,也能给少量液体加热,为试管;②是收集气体的仪器,为集气瓶.
(2)实验室制二氧化碳的原理是碳酸钙与盐酸反应生成氯化钙、水、二氧化碳,方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;用的药品是固体石灰石和液体稀盐酸,反应不需要加热,发生装置用B,二氧化碳溶解于水,密度比空气大,收集装置选C;浓硫酸有吸水性,干燥二氧化碳用浓硫酸,故还需F装置.
(3)装置A是加热固体制氧气的装置,且试管口没有一团棉花,适于加热氯酸钾和二氧化锰混合物制氧气,方程式为:2KClO3
| ||
| △ |
B、氧气不能使紫色石蕊溶液变色,二氧化碳能使紫色石蕊溶液变红色,
C、氧气不能使澄清石灰水变浑,二氧化碳能使澄清石灰水变浑,是可行的,所以错误.
D、氧气能使燃着的木条燃烧更旺,二氧化碳能使燃着的木条熄灭,是可行的,所以错误.
故答案为:(1)①试管;②集气瓶;(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;BFC;(3)2KClO3
| ||
| △ |
点评:气体的制取是初中重要的化学实验之一,既是难重点,又是考查热点,理解反应原理,掌握装置的选择依据、气体的检验、验满、收集方法,了解实验步骤和注意事项是解决该类问题的关键.

练习册系列答案
相关题目